

����GFP��YFP��DsRed֮���ӫ�⵰�ף�FPs���ǿ��ӻ���ϸ����ϸ���ɷֵ�ǿ�ߡ����ǣ���ijЩ����£���ͳFP��ﵽ���ޡ���ͨFP�����ܹ۲쵽�ض�Ŀ�군���ʵĿռ�����ר�õ�������Ⱥ����Ϊ����������ϸ���б����ʱ�ɹ⼤��ɹ�ת���Ϳɹ��л�ӫ�⵰����ýΡ���ӫ�����ij�Ա���Դӷ�ӫ��״̬������Ը����䷢����ף��������Կ���ء��رա���������Щ��ӫ��ӫ��ʡ����о���Ա����ͨ��������������Ŀռ䶨������ֱ�ת����ӫ����������ʱ��仯�IJ�ͬ��������Ⱥ��
ӫ�⵰����һ����Ȥ������ӫ���ʱ������������ʱ��ı��䷢�䲨�����������½�������Щ�Ƿ���ӫ�⵰�ס�
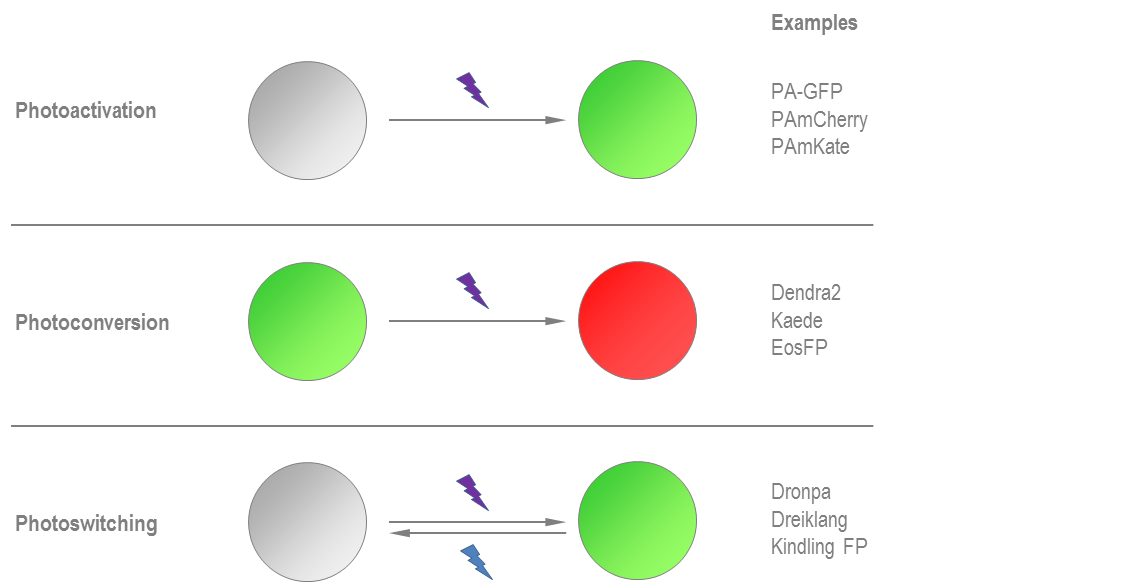
ͼ1��ͨ������/�Ϲ��Ĺ����䣬�ɽ��ɹ�FP��ӫ��״̬�ķ�ӫ��״̬���������ת��FP�ܹ�����ӫ�ⷢ����״�һ�����ֵ����Ϊ��һ�����ֵ����Ҳ����ͨ����¶��һ�������Ĺ�������������ͨ��������ͬ�����Ĺ����������رա��ɹ��л�FP����ѭ��������ִ�����ٴΡ�
�ɽ������״ӵ�ӫ��״̬�����������ϸ�ӫ��״̬��ͨ������/��������ʩ��һ���̵Ĺ����壬�����ڲ���һ���ӵ�ʱ���ڷ��������л������ҿ��Լ�̬ϸ�����̡�����Ȥ����ROI���з��ӵ�ֱ�ӹ������ڼ����Щ�������ϸ���ڵ��˶�������FRAP����������������ʵ��װ���У��������������½���ROI�ĵ����ʺ��ºϳɵķ��ӣ����⼤�����ƹ��������һ�ַ�����
��һ���ɹ⼤��ĵ�����wtGFP���壬��Lippincott-Schwarz��Patterson������������һ������ͻ�䣨T203H��������450��550 nm���������ȷdz��͡�PA- GFP���ɹ⼤�����ɫӫ�⵰�ף������Ϲⱻ�⼤�����������շ�Χ��400 nm�л���504 nm���μ�ͼ2������ˣ���ӫ������Լ������488 nm�IJ�������ʱ���������δ�۵�����100�����ڻ����δ�����֮���γ������Աȡ�
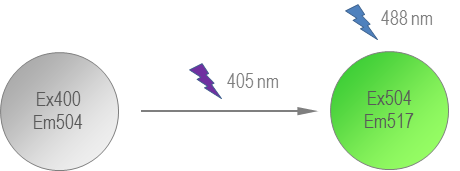
ͼ2��PA-GFP���ɹ⼤�����ɫӫ�⵰�ף����Ա��������ӷ�ӫ��״̬���ӫ��״̬��
PA- GFP������е�DZ�ڹ����ƺ��Dzл�222�йȰ�������Ĺ��յ����ȡ�������̼��������ʧ����ɫ�Ź��ʹ����Ա�Ϊ�������͡�
�˴�Ӧ�ἰ����һ�ֺ�ѡҩ����Phamret�����鵼�Ĺ�������ת�ƣ�������һ������Ĵ�������ӫ�⵰�ף���FRET����Phamret��һ���ںϵ��ף���һ������FRET����ECFP����ż����PA-GFP��ɡ���¶��458 nm�����ᵼ��ECFP��480 nm�����䡣PA- GFP���ڽ�������405 nm���������еġ�֮���ظ���¶��458 nm�ᵼ�¼�����ECFP��PA- GFP֮�䷢��FRET��������ɫӫ�⡣��ˣ�����Ч���͡���Ч����ʽ��������ͬ�ļ��Ⲩ��������ͼ3������������������������ӫ�⵰����ɵĵ��״�С����������ռ����⡣
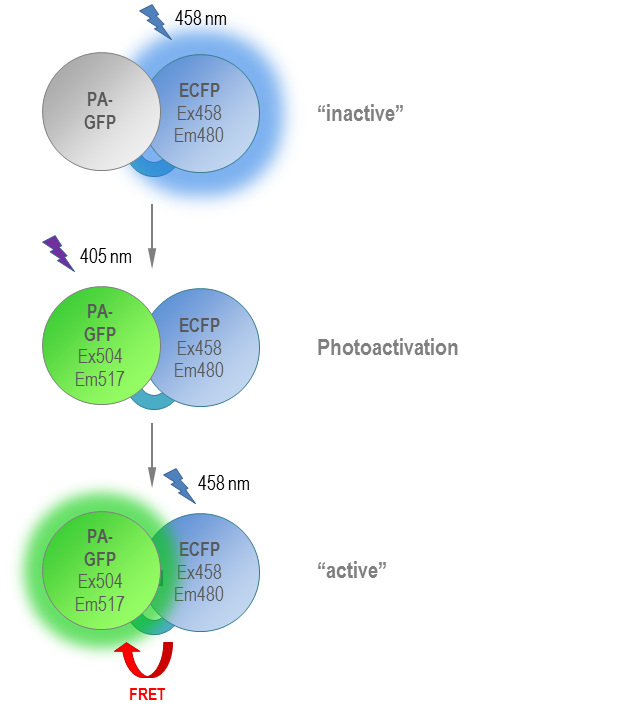
ͼ3��Phamret�����鵼�Ĺ�������ת�ƣ�����PA-GFP����FRET����ECFP��ɵĴ��������塣�����¶��458 nm�ᵼ��ECFP������ɫӫ�⡣ͨ����������PA-GFP���������ֵ�����֮���FRET���ظ���¶��458 nm�ᵼ����ɫӫ�⡣��ˣ�Phamretԭ���������ڿɹ�ת���ĵ����ʣ�������һ���������ɼ������ֲ�ͬ��ӫ��״̬��
ֵ��ע����ǣ���EGFP��ȣ��ɹ��ĵ���ͨ����ʾ�����͵����ȣ�����ʾ�����͵Ĺ��ȶ��ԣ���1����
��ɹ��ĵ������෴���ɹ�ת���ĵ����ʷ�����ӫ���Ѿ�����δת��״̬����ʯ�ʿ�����ɺ��Trachyphyllia geoffroyi�з����˹�ת���������䷢�����ԣ����������߽�����ת�����䷢����������ɫ��Ϊ��ɫ�����ӫ�⵰�ױ�����ΪKaede�����ձ�������Ҷ��[4]�������죬���ǵ���ɫ����ɫ��Ϊ��ɫ�������Kaede����380��400 nm�����Ĺ�ת�������䷢�����ֵ����518 nm��Ϊ582 nm������ʾΪ��ɫ�ͺ�ɫӫ��֮��ı������������ű仯������Ϊ2,000������ת���Dz�����ģ�ͼ4������һ������������Kaede���ľ������ʣ���ʹ���������ڻ�ϸ�������о���FPs�ĵ;ۿ��ܵ��¶Ա�ǵ�Ŀ�ĵ��ף�POI����λ�ú���Ϊ����⡣�ۺ�����������ȫ����POI���������ܡ�
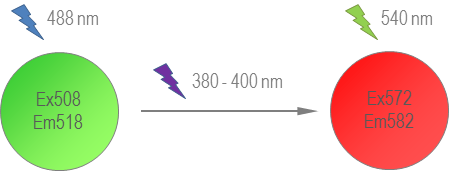
ͼ4��Kaede��ӫ�ⷢ����Դ���ɫת��Ϊ��ɫ��488 nm�������518 nm����ӫ�ⷢ�䡣�����380 nm��400 nm֮��Ĺ����ת������ӫ�ⷢ����ƶ���582 nm��������540 nm��Դ��������ɹ��ĵ�������ȣ��ɹ�ת���ĵ����ʼ���ROI�Ķ��壬��Ϊ���Դ�һ��ʼ�ͽ����ǿ��ӻ���
��ת���Ļ��������ٴ��ǹ��յ����̡�����������£���ɫ���ڲ����鰱��л���His61-Tyr63-Gly64��ͨ�����ձ��ѽ⣬���յ��¸߶ȹ����˫����ϵͳ���γɡ����������ӫ�����ɫ�������ƶ��йء�
��ɫ����ɫ�Ŀ�ת��FP����ɺ��Dendronephtytha sp���������ƺͺ�ɫ�Ŀɼ��������ڱ���ʽDendra�з�ӳ��������ҵ��������Dendra2�ǵ�һ�������ɫ����ɫ�Ĺ�ת�����ס�
��һ���㷺ʹ�õ�ӫ��ӫ�����tdEosFP������Ҫ��ʯɺ��Labophyllia hemprichii�з�������������������ڽ�������������Դ���ɫӫ��ת��Ϊ��ɫӫ�⣬�ܸ������ڳ��ֱ�������������汾mEos��mEos2Ҳ����ˡ�
�ڵ�����ʯ��ɺ����Favia favus�з�����һ�־�����Keade�dz��������ԵĹ��ת�����ס��ڽ�������������ľ���KikGR����ӫ�����ɫ��Ϊ��ɫ�������߶���Kaede�����öࡣ������ҵ����ΪKikume������ͨ��750 nm�����Ķ���Ӽ������й�ת���������������ں���֯������KikGR���ձ䵼�µ�����ʽmKikGR����mEos2��Dendra2һ��ʹ��ʱ����ͨ�������ڳ��ֱ��ʳ���Ĺ�ѧӫ��ʡ�
���Ǵӷ�ӫ��״̬��ӫ��״̬�IJ�����ת����������л������ܹ�����������֮�䴩�����ڲ�ͬ�����Ĺ����壬��Щӫ�⵰���Դر����ٴΣ���������й�Ư�ס�������ӫ��״̬�Ͱ�״̬֮���л��������Ϊ���±�ɫ������Ȼ�ڷdz��͵ķ�Χ�ڣ�������wtGFP�ĵ�����ˮƽ�ϳ��֡�
һ�ֳ��߷ֱ���������ʹ�õ�������֪�Ĺ��л������Ǵ�ʯ��ɺ���л�õģ�Dronpa��һ�ֵ��壬�����������ӣ�ȥ���ӻ�����ɫ�Ŷ���503 nm������һ��������գ���390 nm�����н�С��������ա�������������Ե����ӻ���ɫ�ţ��μ�ͼ5������������ʽ��518 nm��������䣬��������ʽ�����Ϊ��ӫ��̬��
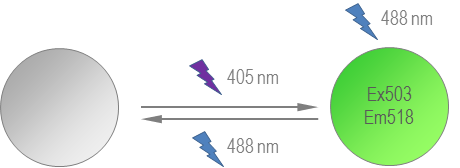
ͼ5��Dronpa��ӫ�ⷢ����Կ���شرա�488 nm�Ĺ⼤��������ɫӫ�⣬ӫ���½���ԽϿ졣�������������������¼���ӫ��״̬��
���⣬�����뷢ɫ�ŵ����ӻ���ص�˳ʽ-��ʽ�칹�����ڷ�ɫ�ŵ�����״̬�£�Tyr66�����ʷ�ʽ���μ�ͼ6����Tyr66��������״̬�¾���˳ʽ��������405 nm������������ʱ��Dronpa����ת��Ϊӫ��˳ʽ����Ȼ��һ��488 nm�ļ������彫Dronpa�����л������ӫ����״̬����ѭ�������ظ����ٴΡ�
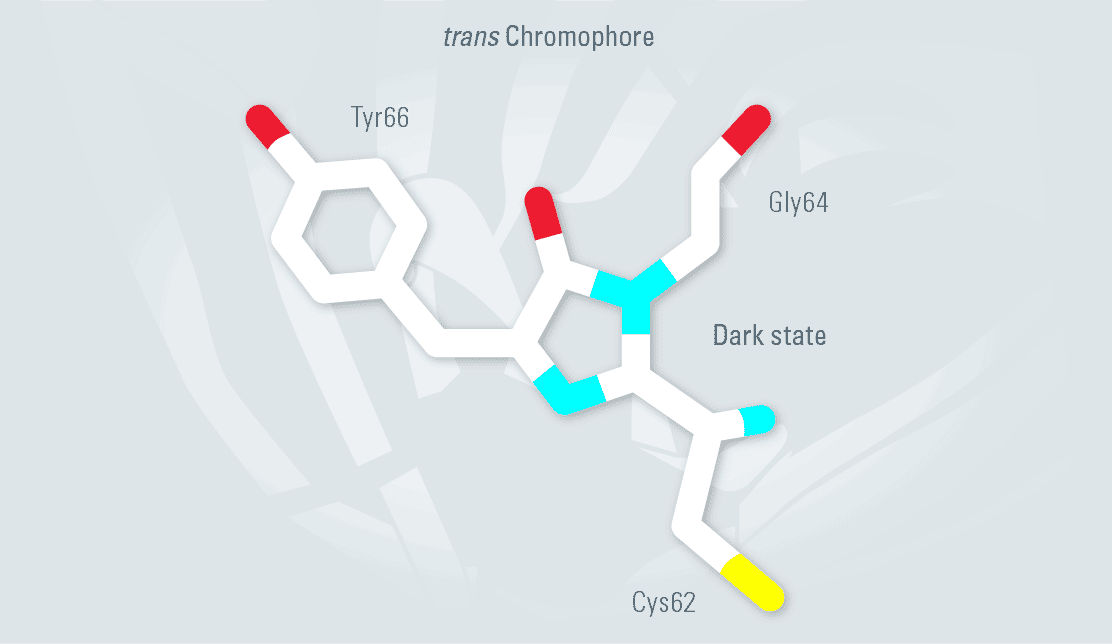
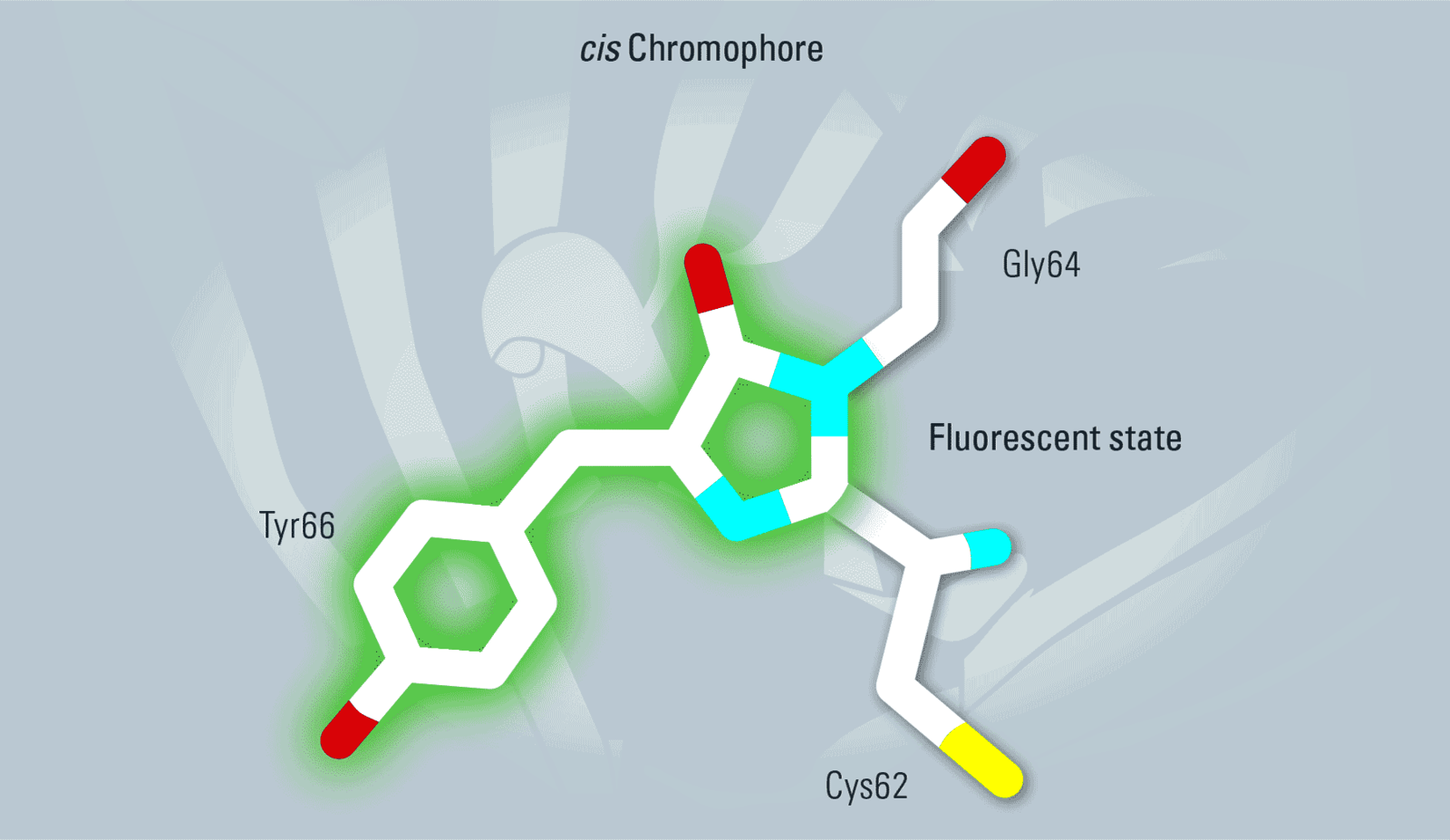
ͼ6��Dronpa��ɫ�ŵ�Tyr66�����ڹ��л������з���˳���칹������Ȼ��ʽ�����Ƿ�ӫ��ģ���˳ʽ����ȴ����ӫ�⡣
�ں�ɫ�����������������ľ۹��л�������Kindling FP��KFP1����
�����µ�ӫ��ӫ��ʵ�����Ŭ���ǽ����һ�ֵ����ʣ��õ����ʽ���ת����ת�������һ��IrisFP��һ��wtEosFP�����������ɫӫ���Լ����ɫӫ����о����п��ؿ��л�״̬�����仰˵�����ø�ǿ��405nm����ʱ��������IrisFP������ɫת�Ƶ���ɫ����״̬��������488 nm����İ����¹ر���ɫIrisFP��405 nm�ĵ�ǿ�ȼ����ٴν������һ���棬��ɫIrisFP��532 nm����رգ����ҿ��Ա�440 nm�����ٴδ�������ʽmIrisFP�����ڽṹΪ��һ����Ӧ�ô��˴��š�
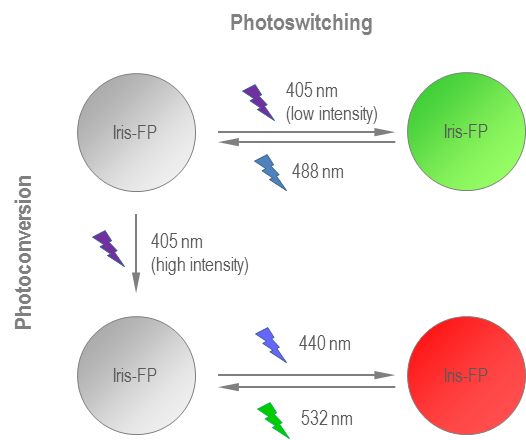
ͼ7��IrisFP�����ת�����ת�������һ���ʵ��Ĵ���������ǿ�ȵ�ѡ�������ӫ��״̬�ͷ�ӫ��״̬֮���л������߽������ʵķ������ɫ����ת��Ϊ��ɫ������
�������ܹ���ݵ�ӫ�⵰���⣬������������ͨ���������������л���ͼ8�������磬�Ի�ϸ������״̬����Ȥ���о���Ա����ѡ��GCaMP��ΪCa 2+ָʾ����GCaMP������Ca 2+��ϸı���ӫ����Ϊ������ӫ�⵰����VSFP1�����ڼ��Ĥ��λ������ɫӫ�⵰��YFP-H148Q��������-���ӡ����⣬��ЩFP������Χ��pHֵ�ı���ӫ�����ԡ�����PHluorin��SEP����pHuji���������ӡ��������ǵİ��������Ը��ٰ��̺Ͱ����¼��Լ�ϸ���ڷ�ѡ�¼���
��ʱ��仯�䷢�����ӫ�⵰�׳�Ϊӫ���ʱ��������Ϊ����pHֵ�仯������ǿ�Ȼ���Ũ�ȵĽ�������Ƕ�������Щ���������������ġ����仰˵����ص����ʵ��������ͨ������ɫ�����ơ�������Щ���ԣ����Բ�����ϸ���ڵ�ʱ���Լ���ʱ���йص��¼���
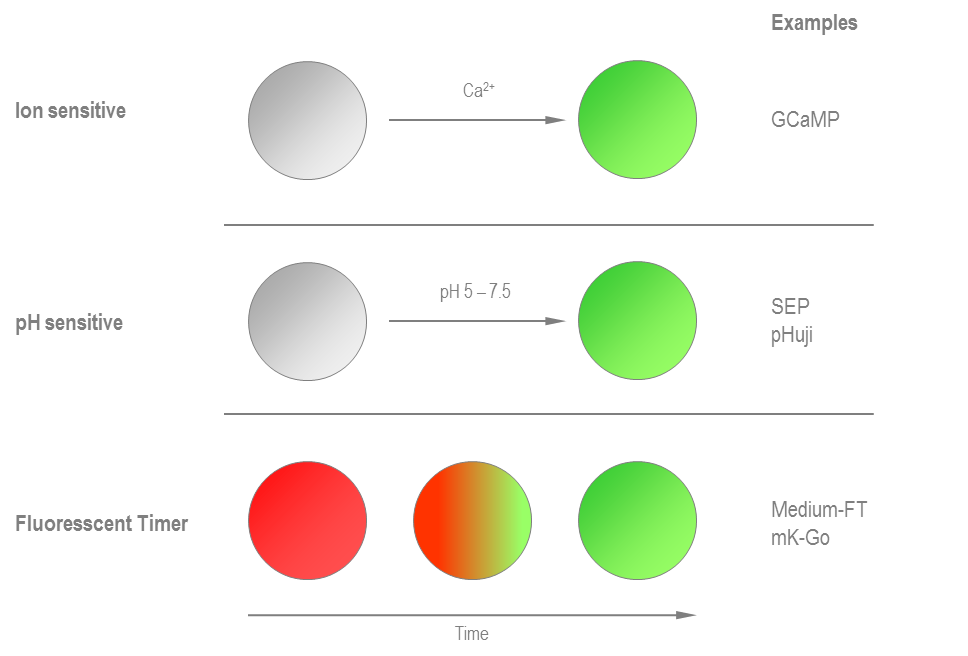
ͼ8���������е�ӫ�⵰���ڽ������ Ca2 +������pH���е�ӫ�⵰�ף�����pHuji����һ����pH��Χ����ʾ�������ӫ��ǿ�ȡ� ӫ���ʱ�����ڰ�ʱ������䷢����ס� �����ǵİ����£��п��ܽ������ʵ������ϸ��λ�ù���������
Sergey A. Lukyanov��ʵ������2000�������˵�һ��ӫ���ʱ���������ΪFT������ӫ���ʱ������DsRedͻ������18Сʱ�ڽ��䷢����״Ӻ�ɫ��Ϊ��ɫ������FT���ľ��壬Vladislav Verkhusha��Ϊ�б�Ҫ���쵥�嵥�塣mCherry���ձ䵼������3�����в�ͬת��ʱ���ӫ�ⶨʱ��������1������Щ�������Կ��٣��еȻ�����ʱ��߶ȴ���ɫ��ɺ�ɫ������Ȼ̫�����������������ڷ�����ϸ�����̡�
Ȼ��������ӫ���ʱ�����п����Կռ��ʱ��ֱ��ʹ۲��ϸ���е����ʵ���Ϊ�����磬���Թ۲쵽�ֻ���ϸ���������̡����⣬�����ٵ�����ת���¼���װ�����Լ�������ԡ���Ӧ���б��϶�������չ������ʾ����ӫ���ʱ����DZ����;��
���� | Exmax(nm) | Emmax(nm) | QY | ���� | pKa | �ṹ�� | ���� |
������ | �������� | ||||||
PA-GFP | 400 | 515 | 0.13 | 2.7 | Monomer | violet | |
PAmCherry | 404 564 | ND 595 | ND 0.46 |
8 |
6.3 | Monomer | 350 �C 400 nm |
PATagRFP | ND 562 | ND 595 | ND 0.38 | ND 25.1 | ND 5.3 | Monomer | violet |
PAmKate | ND 586 | ND 628 | ND 0.18 | ND 4.5 | ND 5.6 | 405 nm | |
Phamret (PA-GFP + ECFP) | 458 | 475 | 0.40 | 13 | Monomer | violet | |
��ת������ | ת������ | ||||||
mClavGR2 | 488 566 | 504 583 | 0.77 0.53 | 14.6 17 | 8 7.3 | Monomer | 405 nm |
mMaple | 489 566 | 505 583 | 0.74 0.56 | 11.1 16.8 | 8.2 7.3 | Monomer | 380 nm |
Dendra2 | 490 | 507 | 0.50 | 22 | 6.6 | Monomer | Initial state |
PS-CFP2 | 400 490 | 468 511 | 0.2 0.23 | 8.6 10.8 | Monomer | violet | |
Meos3.2 | 507 572 | 516 580 | 0.7 0.55 | 53 18 | 5.4 5.8 | Monomer | 405 nm |
Kaede | 508 | 518 | 0.88 | 87 | 5.6 5.6 | Tetramer | Initial state |
EosFP | 506 571 | 516 581 | 0.7 0.55 | Tetramer | |||
mEosFP | 505 569 | 516 581 | 0.64 0.62 | Monomer | |||
mEos2 | 506 | 519 | 0.84 | 47 | 5.6 | Monomer | Initial state |
kikGR (Kikume) | 507 583 | 517 593 | 0.7 0.65 | 37.6 22.8 | 7.8 5.5 | Tetramer | 365 nm |
PSmOrange | 548 636 | 565 662 | 0.51 0.28 | 58 9 | 6.2 5.6 | Monomer | blue-green |
PSmOrange2 | 546 619 | 561 651 | 0.61 0.38 | 31.1 7.2 | 6.6 5.4 | Monomer | 489 nm |
mKikGR | 505 | 515 | 0.69 | 34 | ND | Monomer | Initial state |
��ת������ | �/�������� | ||||||
mTFP0.7 | 453 | 488 | 0.5 | Monomer | 405 nm / 458 nm | ||
PDM1-4 | 503 | 517 | 405 nm / 488 nm | ||||
Dronpa | 503 | 518 | 0.85 | 80.8 | 5.0 | Monomer | violet / blue |
Dronpa-2 | 489 | 515 | 0.28 | Monomer | 405 nm / 488 nm | ||
Dronpa-3 | 489 | 515 | 0.33 | Monomer | 405 nm / 488 nm | ||
bsDronpa | 460 | 504 | 0.5 | Monomer | 405 nm / 488 nm | ||
Padron | 503 | 522 | 0.64 | Monomer | 503 nm / 405 nm | ||
Padron0.9 | 500 | 524 | 500 nm / 400 nm | ||||
Mut2Q | 496 | 507 | 0.28 | Monomer | 405 nm / 478 nm | ||
rsFastLime (DronpaV157G) | 496 | 518 | 0.77 | Monomer | 405 nm / 488 nm | ||
rsKame (DronpaV157L) | 503 | 518 | 0.86 | ||||
Dreiklang | 515 | 529 | 0.41 | 34 | 7.2 | Monomer | 365 nm / 405 nm |
mGeos-M | 503 | 514 | 0.85 | 43.9 | 4.5-5 | Monomer | 405 nm / 488 nm |
EYQ1 | 510 | 524 | 0.72 | Monomer | 405 nm / 514 nm | ||
KFP1 | 590 | 600 | 0.07 | Tetramer | 532 nm / 458 nm | ||
rsCherry | 572 | 610 | 0.02 | Monomer | 550 nm / 450 nm | ||
rsCherryRev | 572 | 608 | 0.005 | Monomer | 450 nm / 550 nm | ||
rsTagRFP | 567 | 585 | 0.11 | Monomer | 445 nm / 570 nm | ||
mApple | 568 | 592 | 0.49 | Monomer | 480 nm / 570 nm | ||
asFP595 | 572 | 595 | <0.001 | Tetramer | 569 nm / 450 nm | ||
Kindling FP (KFP1) | 580 | 600 | 0.07 | 4.1 | ND | Tetramer | green / 450 nm |
rseGFP | 493 | 510 | 0.36 | 16.9 | 6.5 | Monomer | 405 nm / 488 nm |
rseGFP2 | 478 | 503 | 0.3 | 18.4 | 5.8 | Monomer | 408 nm / 478 nm |
��ת��/��ת������ | |||||||
IrisFP | 488 | 516 | 0.43 | 22 | Tetramer | ||
mIrisFP | 486 | 516 | 0.54 | 25 | 5.4 | Monomer | ��ɫ������ɫ�� |
ӫ���ʱ�� | ����ʱ�䣨h�� | ||||||
Slow-FT | 402 | 465 | 0.35 | 12 | 2.6 | Monomer | 9.8 |
Medium-FT | 401 | 464 | 0.41 | 18 | 2.7 | Monomer | 1.2 |
Fast-FT | 403 | 466 | 0.30 | 15 | 2.8 | Monomer | 0.25 |
mK-Go | 500 | 509 | ND | ND | 6.0 | Monomer | 10 |
Exmax������⣬Emmax�������⣬QY�����Ӳ��ʣ����������Ӳ��ʺ�Ħ������ϵ������1,000�ó�
