

ӫ����һ�ֹ��̣��ڸù����У������չ⣨���ӣ������ʷ����ķ���IJ�������ɫ�����ڱ����յĹ�IJ��������Ҹ÷����ڼ���ֹͣ������ֹͣ������������ӫ����������Ӧ�õĻ���Ҫ�ء�
�����ڹ�ѧ������ӫ��ġ����䡱����֮�⣬���컹����ͨ����������ɨ���������ִ�������ͨ���������������ӵIJ�������������Ĺ��ӵļ����������ͬ�ķ���Ч����
ӫ��Ҫô������ѧ��/�����ṹ���Է�ӫ����ʽ���֣�Ҫô������Ⱦ�ϣ�ӫ��Ⱦ�ϣ�ӫ���ǣ�������Ʒ������ν�Ķ���ӫ�����ʽ���֡�Ϊ����������ִ��ӫ�⣬������������Ҫ��ǿ�����Դ����ѹ�����ƣ�±�صƵȣ����㹻�����˹�Ƭϵͳ���˹�Ƭ��������ѡ����ͷ����ķ��䣬��������Ҫ���ǣ�������ӫ��Ĺ�ѧ�����װ�������缯�⾵�������������������ᄉ�����ξ���Ŀ����
�����������ȣ�ӫ���������״�ʹ�����Ͱ����������������ڵ�ʱ��Ӧ�÷�Χ���ޡ��������������֯ѧ��ϸ��ѧ����������ѧ��������ϵ���Ҫ��������ߣ��������۲켼���ĸ����Ľ�������ҲԽ��Խ�����������ӫ���������ĵ���ʱ�䡣
�ڽ�40���Ӧ�úͿ��������У��ü����ѳ�Ϊ����ѧ��ҽѧ����ѧ��ҵ������о������Ļ�������֮һ��Ploem���о�����������Ϊ�����趨�ߵĹ����Լ�Leitz��ǰհ������������������ӫ�������Ľ�չ��Leica Wetzlar�ڿ�������Ĺ�ѧ����ʱ��
�ڱ��ĸ��а�ʱ��˳����������һ��չ���̡�ӫ������������ժҪ���ṩ���й��������ᄉ��ӫ��Ⱦ������Դ������ϵͳ�������Ϣ���漰Ӧ��������漰�˷����ķ�����
ӫ����һ�ַ����������������ں̵ܶ�ʱ�������չ⣨������������ϳ������Ĺ⣨���䣩����ӫ��Ⱦ�����չ�ʱ�������չ�����ʽ���������Ӷ������Ӽ��������ߵ�����״̬�����ӵ����չ��̷dz�Ѹ�٣�����������ص��ϵ͵�����״̬��Ȼ������Ź��ӵķ��䣬����ڿɼ���Χ�ڷ���⣬����Թ۲쵽��
���ֶ��ݵij���ʱ�䣨���룩������������ʽ�ķ��⣨�����⣩���ֿ�����������ͷ����֮��IJ������Ϊ˹�п�˹λ�ơ�˹�п�˹λ�ƴ��ӫ��Ⱦ�Ϻ�����������ӫ�������¹۲��䷢�䡣����������£�С��˹�п�˹λ�ƿ���ʹ�������伤���崦����ӫ��Ⱦ�ϣ��������䷢��崦�۲�ӫ��ɫ��
���۽�����ɨ��ӫ�����������ò����ȷ��������Ĺ��ӽ���˫���Ӽ�����Ȼ��������������������һ��Ĺ��ӽ��뼤��̬��ͬʱ����ڴ��������£��������½�����̬֮ǰ�����������������Ӽ�����ͬ�ļ���̬������ͬ����������ӫ�������������Ӽ���������ӫ�����ơ�
������л����л����Ӿ���ʾӫ�ⷢ�䣬��������ʹ�ø��ܷ��伤��������¡���ֲ�������֯��������UV -light�dz���������ӫ�ⷢ�䣬�۲쵽����Ϊ����ӫ�⣬������ӫ�⡣��Ȼ���ڵ�����ͨ�����зdz����ļ����ͷ�����ס����ŷ�������ѧ�ķ�չ���о��Ѿ������ھ�������ӫ�������Ⱦ���ϣ��������ڿ��ܵ��Է�ӫ�⡣����ѡ���Եض�����ѧ����Ҫ�ķ��ӽ���Ⱦɫ��Ⱦ�ϳ�Ϊӫ��Ⱦ�ϡ����뿹������ż��ʱ�����DZ���Ϊӫ���ǻ�̽�롣���ӫ��Ⱦ���ڹ�����ɫ����ɫ����ɫ����ɫ����ɫ�ͽ�����������з�ֵ���䡣�����ó�ɫ�ͺ�ɫ�⼤��ӫ��Ⱦ�ϣ����ù�籶���ܻ�CCD����ɫ�ͺ���ӫ��-�����ӫ�����������Ѿ��������Ӿ���Χ��ӫ��Ⱦ�ϵļ����ͷ�����ܻ�����ϸ�������ı仯���仯��֮����ѡ��ijЩȾ�ϣ�����Ϊ���ǵļ��������������ϸ���ڽ�����ijЩ���ӵ�Ũ�ȣ�����ƣ��ƺ�pHֵ���ı仯�������仯��
�ع�ӫ����������ʷ�����߿��Բο�Kasten ��������������ֱ����ļ����⣩�Ѿ���Policard��Paillotʹ�á�����������Leitz��˾���������ʿ�ף������غͲ�˾�����䲿�ֵػ�����Ellinger��Hirt�ģ����ֺ�÷�պ�Pick��Haitinger���������ڵ�Leitz��Leica��ӫ����������ϵͳ���й���������ӫ�������ݱ�ĸ�����ϸ��Ϣ�������Rost�Լ����������ӫ������������Ӧ�õ���ɪ��
��������ӫ����������Ҫ������Brumberg��Krylova�������������������������˫ɫ����������������һ���Ĺ�ѧ���ƣ���Ϊ����������ͬ���۹⾵���ᄉ���ж����Ĺ��ᣬ�������������ᄉ�������۹⾵�������۹⾵�����������ж����⡣ʹ�ö�ɫ�Էֹ⾵���������е�ӫ�ⷢ������ʹ�����ӫ������Ҫ���öࡣ���ǣ���Щ�����Բ�δʹ��ҵ�����������ձ��������������Ϊ����ӫ����������������������Ҫԭ��������ڴ����ӫ������Ӧ���У���ⰵ��UV�����Ѿ������˳�ɫ�Ľ�����������������������������������Ե����ơ�ֱ����ʮ������ڣ����ð����۹⾵ʹ�������Ȼ�ǹ�ҵ����
Ȼ�����Է�������ѧ�Ŀ�����������Ȥ�������������ڼ��ϸ������Ҫ����ӵģ�����¡������ķ�չ��Ϊ���о����ִ������ϸ�����е���ϸ��̬ѧλ�ã�Խ��Խ���ʹ�þ��в�ͬ��ɫ��ӫ���ǡ���ͳ������ӫ�������������������������ʺ�ͬʱ���ϸ���еĶ���ӫ��Ⱦ�ϡ�
��Լ��1962�꣬Ploem��ʼ��Schott����������ɫ�������ڷ���������̹⣬��������������ӫ�������������ĵ�һ�ν���[1965]�ͷ���������խ��������̹������������ʱʱ��������֪��Brumberg��Krylova���������������������Ķ���ɫ�������ķ�չ��Leitz��˾Ҳû�У������л���˴������Է������ġ� Opak������������������������������ģ����������·���а���һ�����飬�û�������ĸ��ֱ�����UV������ɫ����������ɫ����ɫ����ɫ�ļ����⡣��ķ˹�ص���ѧ�����ĸ��豸�����������·�����ɽ�����ͬ�Ķ���ɫ��������ͼ1a����������IJ�����˿��������ҿ��ٵظı䡣

ͼ1a��ӫ��ನ���������������ڻ����а�װ���ĸ�����ɫ����������������������ɫ����ɫ����ɫ������������������ڰ�ķ˹�ص���ѧ���죨��¡��1965�꣩��

ͼ1b��Leitzԭ�ͣ�δ��ҵ�����ನ���������������������ĸ���װ�ڻ����ϵĶ���ɫ��������Ploem��1967����

ͼ1c�������ĸ��ɸ����˹�Ƭ�����壨�飩��Leitz������������Kraft��1972�꣩��
�ܿ������ˣ���խ��������̹⼤��Ϊ���㷺ʹ�õ�����ӫ������������ӫ���أ�FITC�������������ļ�������TRITC��������ѿ����ԡ���ɫ����ɫ������ʹ��Ҳʹ��֯�ɷֵ��Է�ӫ����С�������dz��������������������ϣ����Ч����FITC���ڿ�����խ�����⣨ʹ�ð��Ϊ16 nm�Ĵ�϶�˹�Ƭ���������ӽ�490 nm������������������⣩����������ع۲쵽520 nm������ɫӫ��巢�䡣��֯�ɷֵ��Է�ӫ�ⱻ��С����ͼ2a��b�����Ӷ����¸�ͼ��Աȶȡ��ļ���FITC�ӽ���������������ĸ�Ч��������ʹ�ǹ���ѹ����ƣ���������ɫ������Χ��û�к�ǿ�ķ���壬Ҳ����ʹ�á����⣬��ɫ�������ɫ�������������״�ʵ������546 nm��ǿ����������Feulgen-pararosaniline�ļ�����ͼ3a��b����
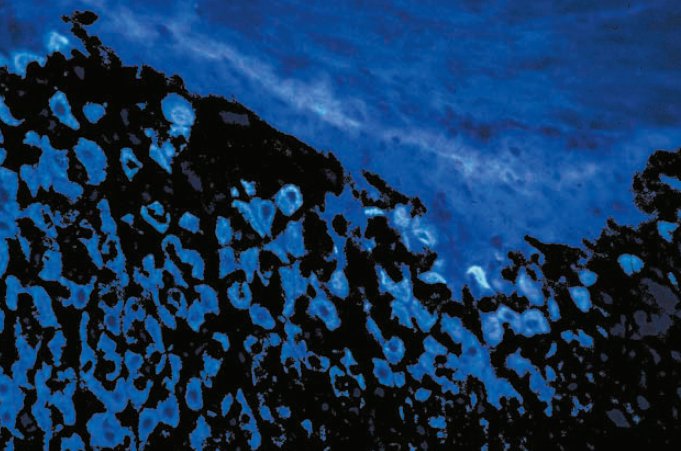
ͼ2a����������߱�ǩ��FITC������֯ϸ������������������������ע����ɫ�Է�ӫ�����֯�ṹ��
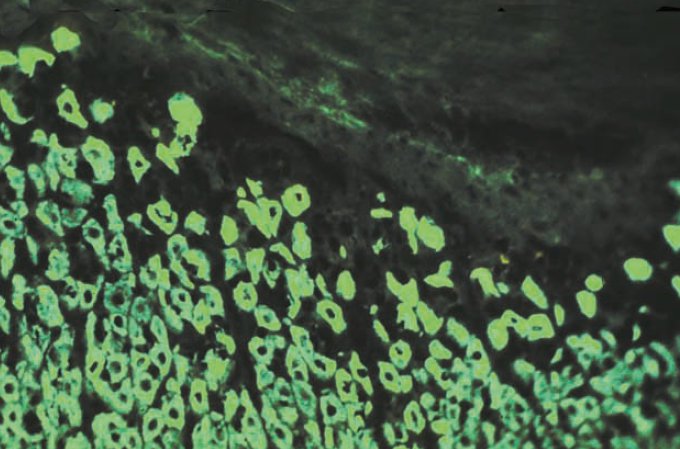
ͼ2b��ʹ��խ����ɫ��490 nm����ͨ��������������Ĵ���FITC��ǩ����ͬ��֯����ͬ����Ⱦɫ��ע�����ӵ�ͼ��Աȶȣ�Ploem��1967����
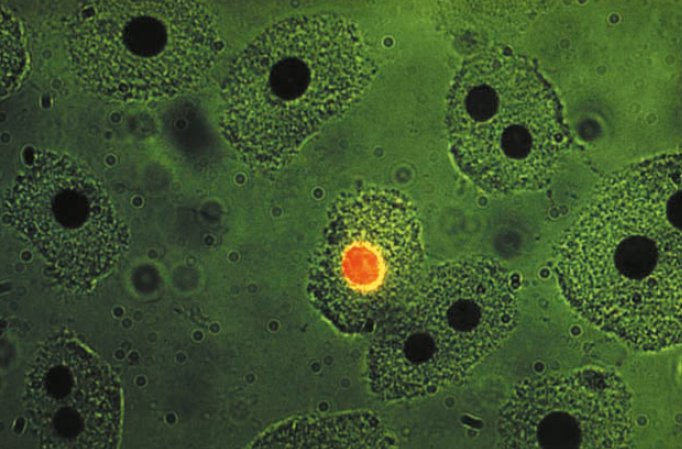
ͼ3a������֯��ϸ������Feulgen-pararosanilinȾɫ�Լ��DNA����������̹���ӻ��������ձ���Ϊ���������գ�������ӫ�⡣ԭ�Ӻ��ϵ�һ���������խ���̹⣨546 nm�����䣬���·�����ɫӫ�⡣
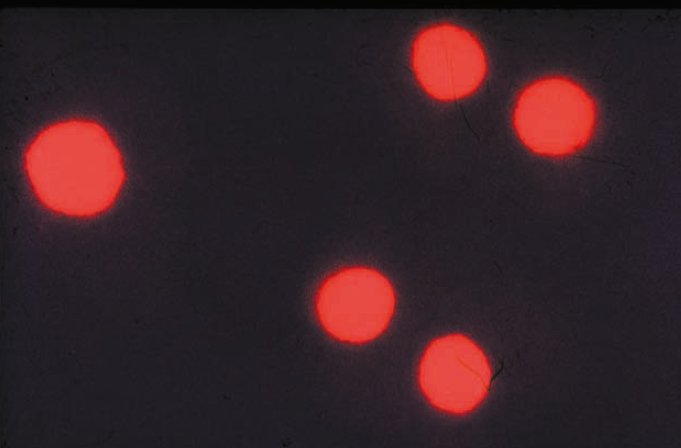
ͼ3b������֯��ϸ������Feulgen-pararosanilineȾɫ�Լ��DNA��������������խ���̹⣨546 nm�������ڷ����̹�Ķ���ɫ�����������������̹⼤�������ĵ�һ�����ӣ�Ploem��1965����ע��ϴ��ͼ��Աȶȡ�
�����ĵڶ������ڶನ�������������ij������У������˴����ĸ�����ɫ�Թ���ɢ�����Leitzԭ�ͣ�ͼ1b����Ploem���Կ϶�Brumberg��Krylova�Ĺ��ס����Ǹ�ʱ�ڣ�����˹�о��IJ��ɼ��ԣ��Լ��ڶ���˹�£�û���κ���Ҫ������ӫ��������ҵ��չ����������Ľ���Ͳ�֪�����ַ�չ��ԭ�����������������������Ŀ�������Ȼ��һЩӦ�����ã���������Leitz�����¼��������Ķ�������Ϊ�����Ѿ����г�ɫ���䰵���������������á�Ȼ������������ӫ��������ҽѧ��Ϻͷ�������ѧ�о��������緶Χ�ڵ�����㷺ʹ�ÿ���������ʹ��������̹��խ���������������������¿����ԡ����ڿ���ʹ�ñ��ĸ�ѹ�����ƣ��������ƺ���һ��ʵ�ʵĽ��顣

ͼ4������ӫ������������Leitz��Leica���˹�Ƭ�����壨�飩�������������˹�Ƭ������ɫ�������ͷ��䣨�赲���˹�Ƭ��
���Leitz������һ����ӱ�Ķನ��ӫ��������������Leitz PLOEMOPAK�����������������ĸ���ת�Ķ���ɫ�ֹ⾵���ֱ��������������Ϲ⣬������̹⡣������������Leitz�������������ĸ�����ɫ���������У��������˹⾵�����ڼ����˹⾵����תת�������գ�����Kraft���������鼤���˹�Ƭ������ɫ�����������ݻ����˹�Ƭ����ϣ���Щ�˹�Ƭһ��װ���˹�飨Ҳ��Ϊ�˹�飩�У�ͼ4�������ڸ������������˹�Ƭ������Ѹ�ٱ�ɹ�·����˶�ͬһ��֯��Ƭ�Ķನ��������Ϊһ��ʵ�ʵĽ��顣���⣬�û����Ը����������е��ĸ��˾������壨ͼ1c����������װ��ͬ���ĸ��˾������壬�������˾��������н���ѡ����Щ�˾����������Ϊ��ͬӦ�ö������ļ����������˾��Ͷ���ɫ����������ϡ�����Ploem�Ľ��飬Leitz�������˴������������ĵ���������ͼ5a��b����

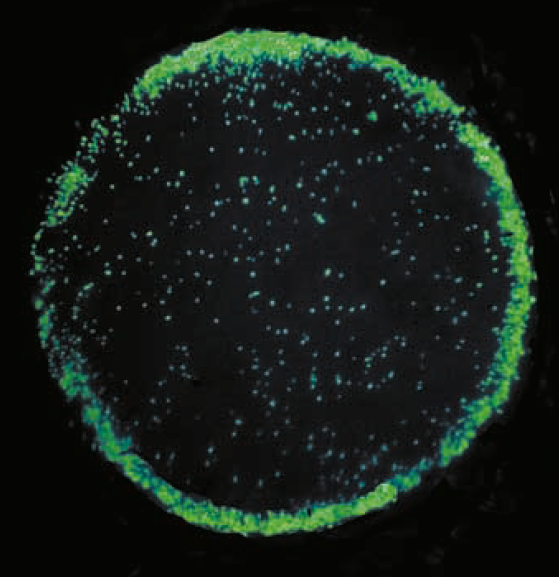
ͼ5a�����жನ��������������Leica����ӫ��������
ͼ5b������ӫ��ϸ����������Ĵ��������ܰ�ϸ����Terasaki®��������������ֲ�о����õ���������������������
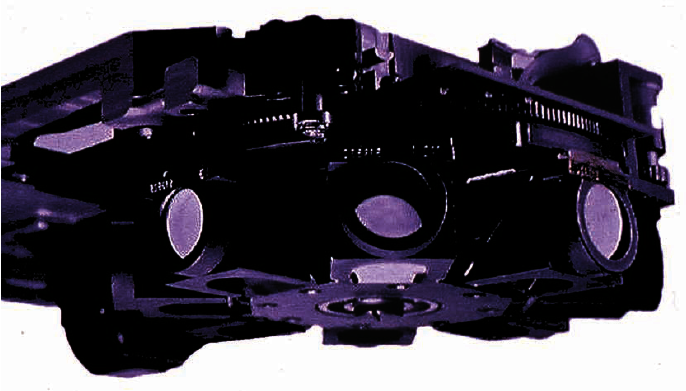
ͼ5c��Leitz��Leica���綯���������������а˸��˹�飨�飩��
Leitz��Leica���˾�������ϵͳ����˸�Ч��������39���Ľ��죬�������������������ʹ���������͵��˾���������жನ��ӫ��������顣��������յ���Leica�з������Զ��ನ��ӫ�������������������������������ڸ��ֲ�����Χ�İ˸��˹�飨ͼ5c���������˾�������֮���л�ʱ�����ڲ�����0������λ��������˿��Ա����ڼ������ʾ���Ϸ���������λ���䱣����35mm��Ƭ�ķֱ���֮�¡�������������������Ⱦɫ���о��е�ӫ��ԭλ�ӽ�������FISH����
Ploem������Ploeg��Ploem���ζ���Ploem��һ��̽��������������ҽѧӦ�ô������Ĺ���������ϡ�������Schott��Leitz������ɵġ�Rygaard��Olson������һ�����͵Ķ̲���������˹�Ƭ�����˹�Ƭ��������кܸߵ����ʣ����Ҷ��ڳ���490 nm�IJ������к�ǿ�Ľ�ֹ������
Ploem����SP�˹�Ƭ��Schott��1 mm GG 455�˹�Ƭ���ʹ�ã��Ӷ���ֹ��UV������������Balzers����һ�����Ƶ��˹�Ƭ��SP 560 = KP 560�������̹⼤����������һ���˹�Ƭ���м��������Ϲ⣨LP 425 = KP 425������һ�ֹ�������Ӧ�������ʵ��о�����ͼ6a��b�У����Թ۲쵽��ɫӫ�⡣
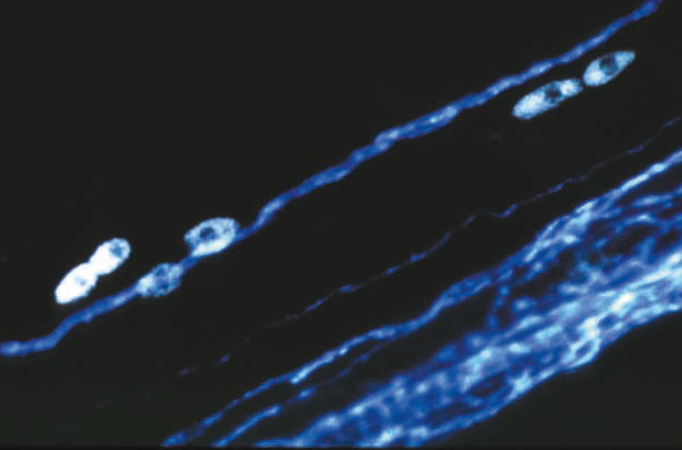
ͼ6a������С��ϵĤ����Χ����ɫӫ�����������ܣ�CA���Ժͻ�ɫӫ��ʴ�ϸ����5-HT������ȩ�յ���CA��5-HTӫ���ŵ�����ӫ�⡣
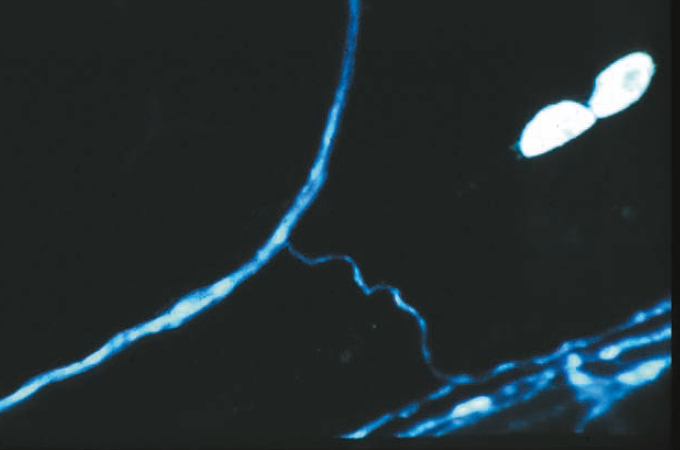
ͼ6b����ͼ6a��ͬ����֯��Ⱦɫ��ʹ��խ��������ɫ�����⣨LP 3mmGG 400��SP��KP��425�����˹�Ƭ������ɫ��495 nm�����Ϲ�������������LP 460 nm�������˹�Ƭ������������������״������۲쵽��ɫӫ�����������������ά�����ɫӫ��ķʴ�ϸ�����Բ�ͬ��Ploem��1971����
�ӹ�ѧ��ҵ�࣬��Щ��չ���ڹ���������ţƤֽ���ֶ��أ����պͺն�����
����������ӫ��������ʹ�õ���Ҫ�˹�Ƭ���������£���a���ڵ¹������г�ΪKP�˹�Ƭ����Ҫ�����˹�ƬLP����ͨ����SP����ͨƬ�����Լ���b�������˹�Ƭ�������Ϲ������ͷ��������������Ҳ������Ϊӫ��ѡ���˹�Ƭ�����磬��Щ�������ƹ۲쵽FITC��520 nm���ķ�ֵӫ�⡣Reichman��ӫ�������˹�Ƭ�����˽��ڵĹ㷺������
Cormane�״�֤��ӫ����FITC��խ��������������������Ƥ������������ӫ���о����ṩ����ѵĶԱȡ����������������⼤������Ƥ���е�����ά������ǿ�ҵ��Է�ӫ�⣬�Ӷ������谭��ӫ�⿹��Ŀ��ӻ���
Leitz����������ӫ����������Ŀ����Թ�������70��������ģ����ͬʱ������ӫ���������������ѧ����������FISH����ҽѧ��Ϻ��о��е�ȫ��Ӧ��Ҳ�����ӡ�Hijmans�ȡ��ǵ�һ��֤������ijЩ���͵���������ϸ���е�ѡ���Լ���µ�Leitz�ನ���������������������ԣ�ʹ�þ�����ɫӫ���ϵĿ���FITC�ͺ�ɫӫ��TRITC������Ӧ����������̹����ֲ����ļ��������Լ�FITC��ֵӫ���ѡ���ɷ����˹�Ƭ��520 nm�����䣨ͼ7����Brandtzaeg��Klein�ȡ���ʹ��Leitz�����������������������£��ڼ�����������ѧ�������Ҫϸ�����ͷ���ȡ�������Ƶķ��֡��ڴ��С�õ��족�γɵ�ѪҺȾɫ�У�ʹ�����������̹������������������������ʾ������ϸ����Χ�ĺ�ϸ����ͼ8����

ͼ7���ÿ���TRITC����Ϳ�IgG FITC����Ⱦɫ�Ĺ���ϸ������խ����ɫ����ɫ������������������°���TRITC��ϸ�����ֺ�ɫӫ�⣬������FITC��ϸ��������ɫӫ�⡣һЩ��Ԫ��ͬʱ����FITC��TRITC��
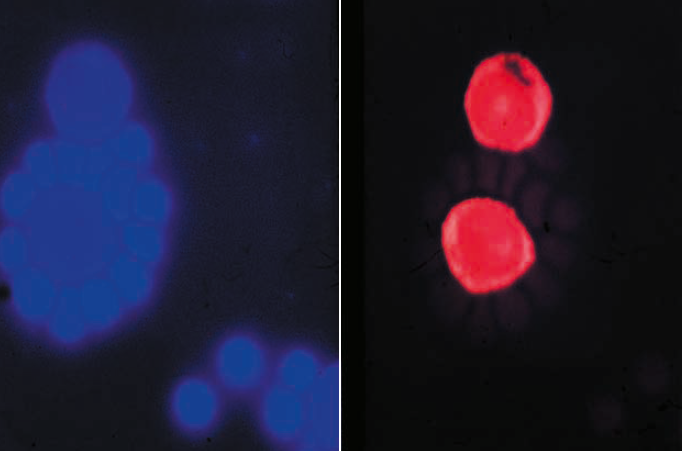
ͼ8����Ѫϸ����õ��족���γɡ�ʹ�������ߵ�������������ϸ��Ⱦ����ɫӫ��Ⱦ�϶�����ϩ���̹⼤�����ܰ�ϸ�����Ⱥ�ɫȾ�����Ⱦɫ��1965�꣩��
�����������У�ʹ�ö���ɫ�������������ƫת����Ʒ�ϡ�����ɫ���Ĺ������Ծ�����ƣ�ʹ��ֻ������ļ�����������ͨ���ᄉ����ƫת����Ʒ�ϣ�������Ҫ�IJ������ɶ���ɫ���䲢�ռ��ڹ������ڶ���ɫ�����档�������ֲ���Ҫ�ļ�����ᵼ����ɢ������ż��٣��Ӷ�����ͼ��Աȶȡ�˫ɫ��������ģ��̲�����������ͨ���ᄉƫת����Ʒ�ϣ����Խϳ���ӫ�Ⲩ�����������˹�Ƭ���赲�˹�Ƭ�����գ����䣩����Ʒ���ᄉ�ľ�Ƭ���淴��ļ����⣬����ӫ��߶�������˿��Ե���Ŀ��������������Ч�����ᄉ��ֵ����NA�����Ĵη���أ����ᄉ���������������������۹⾵��Ȼ���ھ۹⾵�й۲졣�����۵�һ���ನ������������ʱ��ֻ�о��и�NA��0.95��1.30���ĸ߹����ᄉ��x70��x100�����á���ѭPloem�Ľ��飬�����Dz������1.30��NA��ͼ9�����ͽ���40���ᄉ�еȷŴ����ᄉ�������̡����������ᄉ���ر���Ϊ��������ӫ��������Ƶģ��ɲ����dz�������ͼ�Ӷ��ڳ���ӫ���������п�ʵ�ֽ϶̵��ع�ʱ�䡣

ͼ9��Leitz��Leica�����ڣ�1967��ԭ�ͣ��� Versuchs�����ͽ��ᄉx40����NA 1.30����������ӫ����������������ʵ�顣
��������ӫ�������е�һ���������ù�Դ��ͼ���������ᄉ�������ͫ��ͨ������Դ�Ŵ�8�����ҡ�������ָ�ѹ���ƺ�����Ƶĵ绡��С��ͬ�йء����⣬�ᄉ�������ͫ�仯�ܴ����磬����x100��NA 0.90���ᄉ��Ϊ3.6mm������x10��NA 0.30���ᄉ��Ϊ12mm�����⣬���������һ���ֿ��Խ�����ͫ�����õ�ӫ��ǿ�Ƚ����͡����Schönenborn�������DM R��HCS�������������Ѿ����������������·����������������·��Բ�ͬӦ����ʹ�õ��ض���Դ���е��������������������·����Koehler������������ѧϵͳ���ռ�������Ͻ�ʹ�ᄉ�������ͫ�еĹ�Դ�����ڸ������ᄉ����Դ�Ŵ�����ѡ��ֱ��ȡ�����伸�γߴ硣±�صƵĵ���Ӧ�÷dz��ã���Ϊ��˿����Ȧ��Ե�˿ʧ����ɼ��ߵ������ԡ���ô����ʹ����Խϵ͵ķŴ�����
��ijЩӦ���У���DM R��HCS�������У�ӫ��ǿ�ȿ������1.8����������������Χ�ڵĹ�ҵӦ���������������3.5��������������;�ĸ����ʲ�������ɫУ����������������֧����������Χ�����ӡ�����Leica DM R��HCS������ϵͳ������������ģ�飺��HC Fģ���������ѧԪ���ķŴ���Ϊ11.5������HC RFģ�飬�Ŵ���Ϊ4.8�����⣬�DM R��HCS����������֧�ܴ���һ�����������������HC Fģ����ʹ�ã�����25 mm���ӳ��в����dz��ߵ�ӫ��ǿ�Ⱥ����õľ����ԡ���Ҫ�ر�õ�ͬ���Ե��û��������ܻ�����HC Fģ�������������ֻ��������ӫ��ǿ�ȡ��ᄉ�еĹ�Դ��ͼ�������11.5��С����Լ9.5��������Ч�ӳ�����Լ20����Ϊ�˽�һ����߾����ԣ����Խ���ѧ��ɢ�̲���ģ���С���Ȥ���ǣ��Ѿ��۲쵽����ͼ��ǿ�Ȳ�����ȫ�㶨�������½���ͼ���Եʱ���ɻ�����ڹۿ�ӫ�������������ͼ��ӡ�������������۾������Ľ������ν�ġ������ӳ١������෴������ͼ��������ܵ���Ƶ������Ҫ�dz��㶨�������������ͨ����HC RFģ���еĹ�ѧ��ɢ���л�����Ƶģʽ��ʵ�֣��Ӷ��ڴ�Լ16mm�����ij��л�ø��ߵľ��ȶȣ���Ӧ��1/2Ӣ����е�������������������ǵ�����x0 .5����
�����һ��������ӫ���������ᄉ�����е��Է�ӫ�����ʵĹ�ѧ������ѡ����ͼ��Աȶȵ���ǿ��
ӫ��������һ��������������ԽϺ����Ʒ�л��������ͼ����������ʹ�ø���ֵ�����ᄉ����ǰ�ͽ���ƽ�����������ͼ����к�Ӱ�졣�����ᵼ��ͼ�������Ȳ��ߡ�Ȼ����Leica�����۽����������Ըߺ���ʹ�ֱ�ֱ��ʴӱ걾�еļ�����ƽ���ø߷ֱ������������ͼ��
��Ʒ�ж���ӫ��Ⱦ�ϵķ�ɫ��ͨ���������õ��˽�һ�����ơ���ˣ���������������۽�ɨ�������ѳ�Ϊ����ҽѧ�Ͳ����о���ӫ���������ռ����ߡ�
��ȥʮ���У���������ѧӦ�õı�ըʽ������������Ը���Ӧ�õ������������ϵķ�չ�����ڣ���Щ����������װ�ڸ��ֹ����������壨�飩�С�ӫ����������������ͨ���ֶ�������綯����������2-8���˹�Ƭ������ӫ���ӽ��о�������Ҫ�ġ���������Ը��ֹ�����������֧�ֵĶ���Ӧ�ý���ȫ����ϸ�����ۡ��෴���������˹�������ά���ݼ��ؼ��ֵ�ʾ��ͼ��ָ���˿��ܵ�Ӧ�ã���1����
�������õ��������ἰ��ѧ�����ӫ��Ⱦ��ʱ���˴����г����ǡ��ñ��е����Ժ�������������������ĵ��ı���ʹ�õ����б���г��˵���Ĺ���������������߿��Խ��������˲����İ���ȣ�BP����Ϊ+00��/ 00 nm����ʾ���IJ����Ͱ빦�ʴ���������BP 525/20����̲��ͳ����빦�ʵ㣨����BP 450�C490������ͨ�ͳ�ͨ�˲�������ĸSP��LP�Լ���nmΪ��λ�ı��ز���������SP490��LP 520��> 520 nm����ʶ�������������ѧ���������̵IJο������߿��Բο������õ����ס�
�������ᄉ������� | ӫ��ɫ�� | ��Դ | ����ɫ | ��������� |
����ɨ��������LSC��x20 | FITC | 벼��� | 530 + 30 nm& | |
����ӫ������x40 | �� | DCM���� | FT 395�� | 450 + 33 nm&BP�� |
����ӫ������x100 / 0.60�C1.32��SP��KP��630λ��CCD�����ǰ�����赲Զ���ͺ���� | CY3 | ��ɫ515�C560& UV 340�C380& nm BP | LP 580���� | |
����ӫ������x60 / 1.4 | FITC | Ar+-������ | LP OG 530�� | |
����ӫ������x63 / 1.4 | DAPI | ���/������� | ||
ӫ������ | TRITC | ���ش�ͨ�˲���*��MBP�� | ��Ƶ�ٷֱ� | �����䣩 |
ӫ������x100 / 1.35 | LB | ����100W BP 460�C449& BP 460�C490& |
| �����䣩 |
ӫ������ |
| ����100 W |
| �����䣩 |
�綯����������x100 / 1.3�� |
| ����100 W | �ĸ�����������@��FC�� | �����䣩 |
����ӫ��������CCD | DAPI | ������ BP 450�C490& BP 546/12& | ���� | |
����ӫ�������ͣ�CCD��x40 / 0.75 |
| ���ͨ�˲�����MBP�� | ��ͨ����ɫ����������PBS����〜 | ��ͨ�������˲��� |
���е綯�������������ӳٷ�������CCD��ӫ��������x63 / 1.32 | cascade bl F | ����100 W | A@ HQ-FITC@ HQ-TRITC@ HQ-Cy5@ HQ-Cy7@ DBS 580@ nm |
|
���е綯�˾���������CCD����ͷ��ӫ������FISH Morrison��Legator�е� | DNA̽�룺 | BP&510/20 nm | ��ͨ����ɫ����������PBS����〜 | ��ͨ��ͨ�ķ����˹�Ƭ�� |
����CCD�������ӫ������ |
| ����50 W | ��ͨ��ͨ�����˲��� | |
ӫ��������CCD�����x20 / 0.75 |
| ����100 W |
|
|
����CCD�����������x30 / 0.5 |
| �ֶ�������ӫ���˹�Ƭ������λ�û��� | ||
ʹ�ö�ɫ������ |
| ����100 W | ��ɫPBS�� |
|
*������ߡ�
^�̲�SP��KP�������˲�����
��խ��ͨ��BP�������˲�����
〜���ͨ�˲�����MBP����
������ɫ��������DBS�������ɫ����DM����
��〜��ɫ��������PBS����
�����Ϲ�������LP����
$�����ͨ��BP�������˲����ͷ�����ͨ�˲�����MBP����
@�����������壬�飨FC����
����������������ķ�չ�Ѿ������˽�һ���ķ�չ������Ա�����������Ա������ӱ��г������������߱�ǣ������������ø-DAB�����߽�-������������ø���ı걾���ṩ��ǿ�źţ�ͼ10��11��������
���Ի��ǿ����ź�-��ͼ��Աȶȣ����Ҿ۽�ǰ�;۽���ͼ������ή��ͼ������-�������RCM�������������۹�ѧ������ʵ�ֹ�ѧ�����ֱ�������ѧ������Զ���Ϊ��������ͼ��
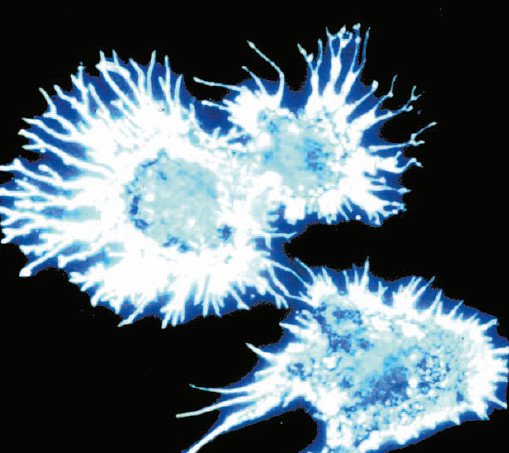
ͼ10������Ա�������RCM����С��Ĥ����ϸ��ճ���ڸDz�Ƭ�ϣ�������Ա��濹ԭ�ĵ���¡����Ⱦɫ�����߹�������øȾɫ������DABox��Ʒ��ǿ��Ӱ�죬�ɼ���˿״α���ϸС���죬������Ұ�������Dz��ɼ��ġ�
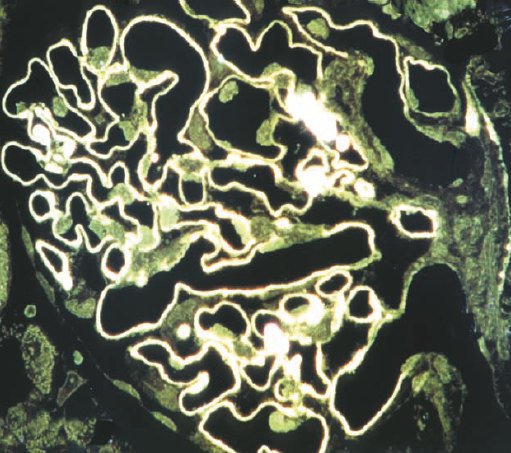
ͼ11��������֯�ij�����Ƭ��Լ35 nm������������øDABȾɫ������Ա������۲쵽����С�������Ⱦɫģʽͨ����ӫ�������۲��������ͼ��

ͼ12�����ڷ���Ա��������˹�Ƭ�����壨�飩������һ��ƫ������һ�����ԣ�50������������һ�������ǡ����Խ�����˹�飨�飩����Leica Epi��������һ��λ���Խ���ӫ���������
���������Ⱦɫ��ǿ�ҷ����ṩ�˺ܸߵĶԱȶȣ���˸�Ⱦɫ���������ྭ��ģ������ԣ���֯��ѧȾɫ���ϣ�������ʾ�е�ǿ�ȷ������Ҫ����ӡ���һ��Ⱦɫ��ͨ���������ṩ���õ���̬ѧȡ��������������£����ʹ��ӫ��������ȣ����Ի�ø���ȷ�����߱����λ�á����⣬����ͨ���������������һ��������Ƭ��������ͬ������Ⱦɫ������EMȷ�����ֹ�ѧ�����۲졣
�ڹ��۽�����ɨ�������У�����ͨ�����������������ɢ�⣬�������������ᄉ������������ɢ��Ĺ�ѧ��ʩ����ִ��RCM�����������������Ⱦɫ�����ǿ�ҵļ��ⷴ�䣬������ɫ�dz����ޡ�����ͨ������ʹ�ý�С����׳ߴ磨����10�ף����óߴ�ȹ��۽�ӫ�⼤��ɨ�������д����ӫ��Ⱦ�ϵ���׳ߴ�СԼ�嵽ʮ������ˣ�ʹ�÷������߱�ǿ��Ե��¹�ѧ�ֱ��ʵ�������ߡ��걾��ӫ��Ⱦ�Ϻ�Leica�����۽�����ɨ������˫��Ⱦɫ��Ϊ���ֱ���ṩ���µĿ����ԣ��������ɼ�鷴�������߱�ǡ�
RCMʹ��ӫ������֧�ܣ�������������ѹ�ơ���ӫ�������������У��������һ�������ƫ���˹⾵�����壬���а���һ��ƫ�����侵��һ����ƫ����ͼ12����ͬ��������Աȶȣ�RC������ģ�飨�����������ϵͳ��Ҳ������������·����RCĤƬģ�������ڴ������뵲���/���ȦĤƬ�Ļ���װ�á����⣬Ϊ����Ա����������������ᄉ��Leica RC M-plan�ͽ�ʽx100 / 1.25 RCM�ᄉ����ǰ����װ�Ц�/ 4�壬Ӧ���ӵ��ᄉ�飨����ӫ���������ϡ��ᄉ������ǹ��������
�ڷ���������У��ԱȶȻ��ڷ���ǿ�ȣ�=�����ʣ��IJ��졣���������͵������У�Ӧ����ע����ǣ���ķ��䷢����ÿ����ѧ�߽紦�����������ʺ�/�������ʷ����仯ʱ��������ʾ��С��1���Ҵ����С��0.2���ķ����ʵ���������������������Ͳ�ڲ��к��ķ��䣬�����������ó���������÷����ͼ���ڷ���Ա������У����ַ�����������ڼ�������ɢ��������ѣ�⡣ͨ���������������װ����������Ŀ������������ᄉ�ĺ�����ƽ�湲���ƽ�����������·���в���һ�����οף�����Ϊ�ڶ��ַ�����ͨ��ʹ�á� antiflex�����������˲���Ҫ��ɢ�䷴��⡣ʹ�ý���ƫ�⾵�����������ڲ�����Ĺ⣬���ֻ�д���Ʒ����Ĺ���ܴ��ݵ��۾���Ϊ��Ŀ�ģ����ᄉ��ǰ����Ϊ�ᄉ�ṩ��һ���ķ�֮һ��Ƭ����ͨ����/ 4�壨���µ�����Ʒ��������Ʒ��������ϣ���ʹ���ƫ����ı�Ϊ2 x 45��= 90�㡣
