

����ӫ�⣨IF����һ�ֿ��ӻ�ϸ���ڹ��̣������ͽṹ��ǿ����IF�Ƽ�����ͨ��������������������CLSM��Epifluorescence��TIRF��GSDIM�����з���������ȡ����Ӧ�ó�����о���Ա����Ȥ��ͬʱ��IF�������ٿ���ʹ�ü�ӫ�������Ĵ����о�����˵�ѳ�Ϊ�ز����ٵġ�
IFʵ��ĺ�����������ͬ�������ϣ�
�����ȣ������Կ���������γ����߸�����Ա��ϸ��������ķ��ӣ�����������Ϊ�����ʣ���
���ڶ��������߸�����ż����ӫ��Ⱦ�ϣ�����������������п��Կ���Ŀ��ṹ��
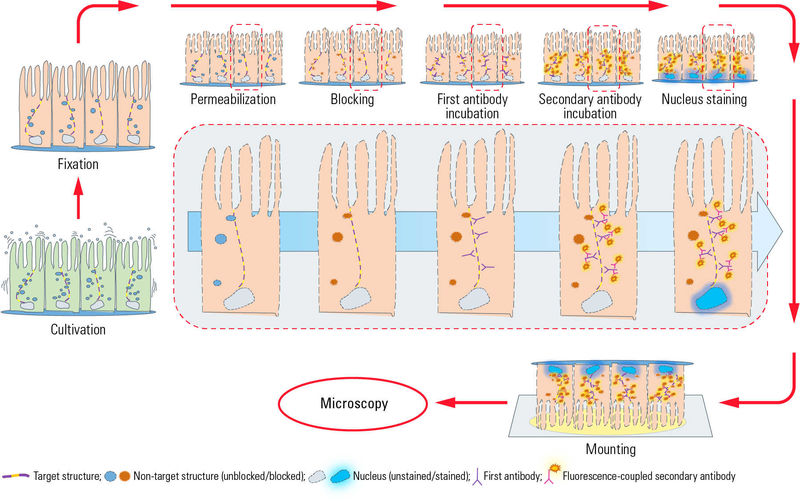
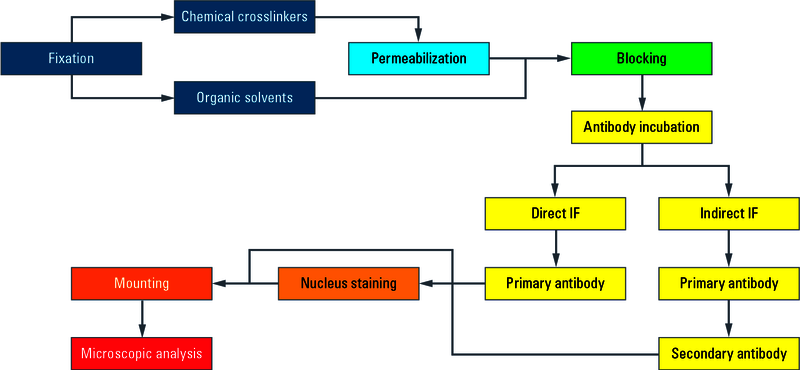
ͼ1����ͼ˵���˼��IF�ĵ��������̣�������Ƥϸ��ճ���ڸDz�Ƭ������������������ϸ���õ���������û�ѧ�����������ȩ��ɱ��������������ȥ�ۼ����������裬��ʹ�����ܹ�����ϸ��Ĥ��������Ѫ�壬�̷ۻ�ţѪ�����տɼ��ٿ�����ǰб�ṹ�ķ������Խ�ϣ��Ӷ����̶ȵؼ��ټ������źš��������������һ������������ÿ���������ʶ��з����ϵı�λ���ڵڶ������������У�ӫ����ϵڶ������ǽ��ʩ�ӵ���һ���壬��˿��ӻ��нṹ������������ò��뵽DNA�е�Ⱦ�ϣ�����DAPI��Hoechst������ϸ����Ⱦɫ���ڽ��Dz�Ƭ�̶����ʣ�����Mowiol��Prolong Gold���̶��������ز�Ƭ��֮��IF�Ƽ����ɽ���������顣
����ʵ������ͣ������ֲ�ͬ��IF���壺��ֱ��IF��һ��IF�У���ӫ��Ⱦ�����ӵ�������һ����������ڽ�ϰб�ṹ��ֱ�ӿ��ӻ���
�ڵڶ��ַ�ʽ�У���Ϊ��ӻ����IF�������������������ȣ��ض���һ��ʶ��б�ṹ��Ȼ��Ӧ�����һ���������Խ�ϵ�ӫ��Ⱦ��ż���ĵڶ����塣ͨ�����ڶ����嵼�������һ�����������������������ԣ�����Ŀ����ӫ��Ⱦ�ϣ����Ƚ�������IF���壬����ÿ�����в�ͬ����ȱ�㣺
ͨ����һ����ӫ��Ⱦ��ż����ֱ�ӵ�IF�ȼ�ӵ�IF���죬��Ϊʡȥ�˷�ʱ��ϴ�Ӻͷ������衣��ˣ�ֱ����Ƶ�����ڴ���������ʺ��ڱ�����Ƶʵ���У��������ٴ�ʵ���У�����Ʒ���п��ٷ��������ǣ�����ʹ�öԿ�ԭ���и������Ĺ������õ�һ����ͬʱ��Ҳ��һ�������ķ��棬��Ϊӫ��ż������֤��һ���۸��⣬����ҪΪÿ���нṹʹ�õ�����һ������������IF��ȣ�ֱ��IF�п�����ӫ��Ⱦ�ϵ����ӻ����������ʵ�������ԡ�
����������Ǽ��IF���������ơ�ͨ������һ��IF��Ӧ�����У�ͬһ��Ʒ�еļ�����ͬ�б�ṹ��Ҫ���ӻ�����˱���Ϊÿ���б����ѡ��������ӫ��Ⱦ�ϡ��ڼ��IF�У����Խ���ͬ��ӫ��ż�������벻ͬ��һ�����ʹ�ã���ȻҪ�������ֵķ�Ӧ�ԣ����෴�����Ҫ��ֱ��IF�С��桱Ŀ��ṹ����ɫ��ϣ���ÿ����ɫ����Ҫһ��������һ������ӷ�������һ���ŵ���ͨ�����������źŷŴ���������ӿ���һ��һ����ϣ��Ӷ�����ӫ����ǿ������ζ�ű���ʹ�ý��ٵ�һ����
���IF�Ĺ������̿��ܻỨ�Ѹ���ʱ�䣬��������һ���Ͷ����Ŀ�������Լ�ͨ�������õķ��������Ǵ�����о���Ա����ѡ������
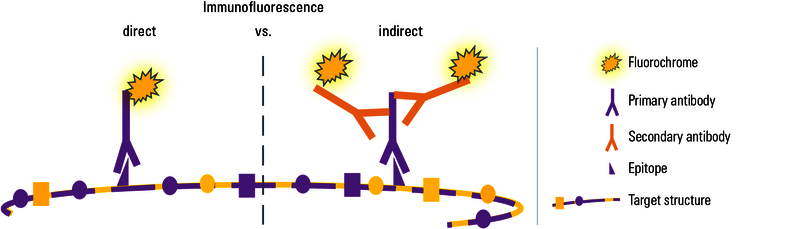
ͼ2��ͨ������ӫ��۲�нṹ�ķ��������֣������ֱ����У���ʹ���ض��ĵ�һ����ʶ��з����ϵ��ض���λ���ڴˣ��з����ɼ�����ͬ�ĵ������ǻ���=����ӣ���ɣ��������ÿ���ǻ��Ͼ����ֳ�������ͬ���͵ı�λ��Ϊ�˼����������һ����λ��
��ֱ��IF�У���һ����ֱ��������ӫ��Ⱦ�ϣ���ӫ��Ⱦ���������¿��ӻ��б�ṹ��
�ڼ��IF�������Ա�ǵ�һ����ĵڶ�����������Ӧ��ӫ��ż���ĵڶ����塣���ڼ�������������ӿ��Խ��һ��һ�����壬�����ѡ�����ӫ��Ⱦ�Ϸ�����и��������ԣ����һ������źŷŴ�
��������IFȾɫ��ؼ��Ĺ����Ǻõ�һ����ͬʱ�����ڼ���ÿ��ϸ�������е�ÿ�ֵ����ʣ�һ�ֻ�ʲ�����ֿ��̹��Ŀ����ǿ��õġ����ǣ�������Ҫע��һЩ�dz���Ҫ�����顣
Ҫ��������IFȾɫ������ȷ�Ŀ�ѧ���ٴ�������������ȷ��һ������п�ԭ�������ԡ�������ʱ������Ӧ��������ҵ�ṩ�̵����������ݹ��ڸ�������������Ѿ�ʹ�ò�������֤�ĵ�һ����ѡ���塣�����������վ�Ͽ�������ݱ����Ի�ȡIFȾɫ�Ŀ���ͼƬ�������������������������ѷ����IJ�ͼ���бȽϡ���ע�⿹��Ŀ�¡�ԣ���Ϊ����¡����������Խ��һ����λ�������¡�����ʶ������λ����˸����ܶԷǰб�ṹ���з������Ա�ǡ���ˣ�
���Ҫִ�ж�ɫ���IF����ͬ��һ���������Բ�ͬ���֣�����ͨ�������ӫ��ż���Ķ������б�����������߸������μ���1�������磬��������Դ��С��Ŀ��忹����A���������ӵĿ��忹����B�����Դ���Ŀ��忹����C����IF��ѡ�����ʱ���������ס�����Ǹ���ֻ��������ʶ��һ��һ�������⣬��������������ĸ�ʵ���е�ӫ��Ⱦ�ϱ����ڲ������ϲ�ͬ��������������������ӫ���źš�����Թ����벨����Χ�������ߵ������ӫ��Ⱦ�����ӵĶ�������Լ����κ����ֵ�һ������ˣ��о���Ա���ܿ������õ������������˹�Ƭ�飬��������������
 |  |  | |
|---|---|---|---|
| ��� | ����A | ����B | ����C |
| Ŀ������ | �˵� | �˵� | �˵� |
| һ�� | ������A | ������B | ������C |
| һ�����ַ�Ӧ�� | ������ | �ÿ����� | �������� |
| ������Ӧ�� | ɽ����� | ɽ���� | ɽ���� |
| ӫ��Ⱦ�ϼ���/���� | 490/525���� | 556/573���� | 650/665���� |
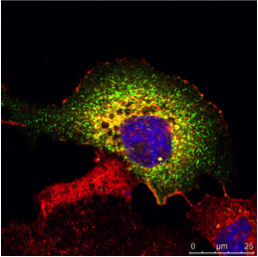
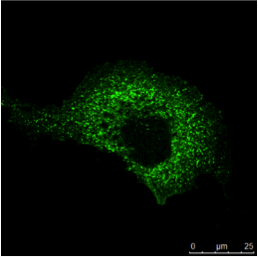
���� ����A
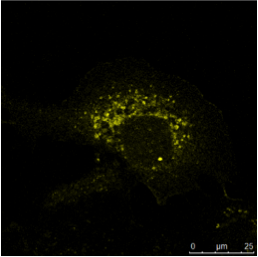
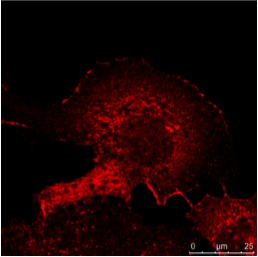
����B ����C
��ǩ1���˶�ɫ���IF��ʾ����ʾ�������ͬһϸ����ͬʱ������ֲ�ͬ�ĵ����ʡ�Ϊ��ʹ�����ֲ�ͬ��ӫ��Ⱦ��ż���Ķ���������ǣ�������һ����������Բ�ͬ�����֡�Ϊ���������н��ж��صķ�����������ӫ��Ⱦ�ϵIJ������ױ��벻ͬ����Ʒͼ��������ϸ��Ҳ��Hoechst 33342�����Խ���ϸ����Ⱦɫ��������Leica TCS SP2�Ͻ��С�
IFЭ�������ڸ��ֲ�ͬ����������Ʒ�������õķ����Ǵ�ϸ���������ж������ģ���ˣ�ϸ������Ⱦɫ��ճ��������ϸ�����Խ����ڸDz�Ƭ����ײ������ϻ�ֱ�ӽ����ڲ������������ϣ���������ʱ������IF���ڽ�ϸ��ʩ�ӵ�Ŀ�겣Ƭ�Ϻ�����ͨ��cytospin������ϸ��Ҳ���Խ���IF��������������£��ص㶼�Ƿ���ϸ���ڹ��̻�ṹ���ⱻ��Ϊ����ϸ����ѧ��ICC����
��һ���棬��������֯��ѧ��IHC���У�����֯�ض�������¼�鵰���ʻ���ӵĴ��ڡ�����������Ƽ��ij�����Ƭ��ͨ��������ʯ���У����������о��뻼����������ڽ��������е����ʵı����������֯��Ƭ�⣬�����Զ��������������IF����һ���̳�Ϊ�����尲װIHC����Ϊ�����Ŀ�ģ���ͬ��ģʽ������С��������������磬��ֲ��ģʽ����ȵ���̥���Ͻ����Ͻ汻ʹ�á�������IHC��һ���������ߴ����ص�IF�Լ�����ȵ����ơ������ķ��������������ϸ��Ⱦɫ��Ҫ������ʱ�䡣���⣬�������䱸�������ڷ����������������ѧ�豸��������
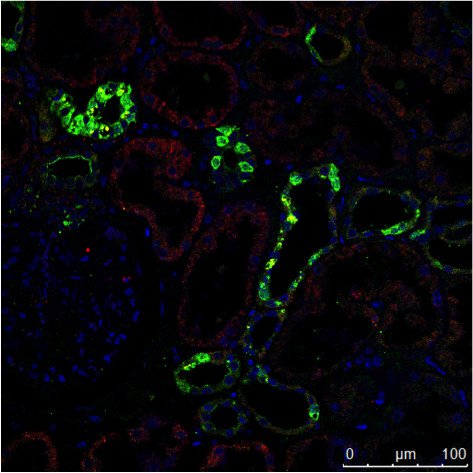
ͼ3��a���������������֯��ѧ��IHC��Ⱦɫ��ʾ��ͬ�ṹ�����磬��С����С�ܣ�Զ��С�ܣ���ϸ�����Ͳ�ͬ������ɫӫ��Ⱦ�ϱ�ǵĵ����ʵı���������ض���ϸ�����ͣ�����ɫ��ǵĵ�������㷺���
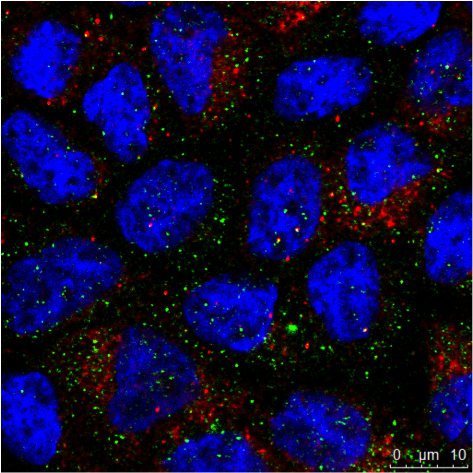
b������ϸ����ѧ��ICC��ͼ����ʾͨ�����IF��ͬһ����ϸ����MDCK���е����ֵ�����Ⱦɫ������������ܽ�����֯�������о�������Ҫ�������ֵ����Ƿ�λ��ͬһ�ṹ�С�������Ʒ����Hoechst 33342�����Խ��к�Ⱦɫ��������Leica TCS SP2�Ͻ��С�
����Ƶ������Ӧ�ر�ע��ϴ�Ӳ��裬��Ϊͨ���ʵ���ϴ�ӿ��������Ƶ������PBS�DZ���ϴ�ӻ���Һ��������PBS ++��PBS-T֮��ı���Ҳ���ձ顣PBS ++����1 mM CaCl 2��MgCl 2�����Ʋ���з�ֹϸ�������Ĥ�ȶ����á�����PBS-T��Ϊ����߿���Ľ�������ԣ�����Ũ��Ϊ0.05����ϴ�Ӽ�����20�����ӡ�С��ͿĨ����ȡϴ�ӻ���Һ�dz���Ҫ������ʹϸ����������������Dz�Ƭ����������㹻��ʱ�䣬���ڳ�������֮��ȴ������ӣ���ȷ��ϴ�ӻ���Һ��Ч��ɢ�������С�IF����ĸ�����ϴ����������ı�Э�����г���
����IF��Ӧ�ĸ��������������¡�����ĩβ������������ϸ�����IF���������ı�Э�顣
�̶�����Ƶ����ĵ�һ����Ŀ����ʹϸ����ϸ���γɻ���֯�����䵱ǰ״̬�����ڽϳ���ʱ����ͨ����ѧ�Լ������Ƽ����ڹ̶������У���Ҫ����ϸ���ṹӦ�����ܱ�������Ȼ����ͬ�Ĺ̶�����������IF��ÿ���Լ���һ���ı�λ�в�ͬ�����á�������λ����ܱ��̶��ڸǻ��������IFȾɫ������������ÿ�ֿ��������ڸ��̶ֹ�������ķ�ʽ��ͬ�ؽ���俹ԭ������б�Ҫ���Լ�������¿���Ĺ̶�������ͨ���������ڿ�������ݱ����ҵ����ʵĹ̶����Ĺ������Ĺ̶������ɱ���ϸ������ϸ���ṹ����Ϊ��ԭ�����ý���ṩ���谭�Ŀ�ԭ��ʵ���ϣ�������������֮��ȡ��ƽ�⡣
�̶����ɴ��·�Ϊ���ࣺ��ѧ���������л��ܼ���
��ѧ�������������ȩͨ�������백�������ĵ����ʣ��ڴ��������£�ϸ����̬���ܺõر��档���ǣ���ԭҲ�ǽ����ģ����ܻ���ٿ���Ľ�ϡ����ȩ��ϸ���ṹҲ���з������ã����������»ᵼ�±걾�ĸ��Է�ӫ�⣨����ġ����ա�����
����״����֮ͪ����л��ܼ������������ò����������ʣ��Ӷ�����̶�����ϸ���ڡ��������ס�������Է��Ӻ�����֬�ʳɷֻ��ڴ˹����ж�ʧ��ͨ����ʹ�ü״��ͱ�ͪ����ϣ���Ϊ���ܼ״����ʺϱ���ϸ���ṹ�������������λ���м��䲻����Ӱ�졣��ͪ���������С������Ӧ�ÿ��ǵ����Ѿ�������ϸ���е�ӫ�⵰�ף���GFP���������л��ܼ��̶����ںܴ�̶��ϱ��ƻ������һ���������̲�����ʹ�ù̶�����������������4����ȩ��ʼ10���Ӽ��������ڸ���ϸ��ϵ�Ϳ�ԭ��
| �̶��� | Ӱ�� | �ŵ� | ȱ�� | |
| ��ѧ������ | ��ȩ | ͨ�������백������������ | �������õ�ϸ����̬�� �������Ѿ����ڵ�ӫ�⵰�ס� | ��ԭҲ�����ǽ����� |
| ���ȩ | �������õ�ϸ����̬�� �������Ѿ����ڵ�ӫ�⵰�ס� | ��ԭҲ���ܱ����� ���Է�ӫ�� | ||
| �л��ܼ� | �״� | ͨ������̶��͵����ʳ����� ϸ����ͬʱ������ | ���ñ��������ϵ�ṹ�� �뻯ѧ��������ȣ�������졣 | �������λ��ǿ�ҵĸ���Ӱ�졣 ���ʺ�ӫ�⵰�ס� �����Ժ�֬�ʳɷ�������ʧ�� |
| ��ͪ | �Ա�λ����С�� ����ij��� | ���ʺ�ӫ�⵰�ס� �����Ժ�֬�ʳɷ�������ʧ�� |
��ǩ2���̶��Լ�
ͨ��ͨ�ԣ�����������ϸ���ڽṹ�������彫������ϸ����֬��Ĥ�����ݹ̶����͵IJ�ͬ����Ҫһ��������ͨ���衣�����л��ܼ��̶�ʱ��ϸ��Ĥ�Ѿ���ÿ�����������ֱ�ӽ��з�ա��û�ѧ�������̶���ϸ����Ҫʹ��ȥ�ۼ����ж������ʵ��ͨ�ԡ�����ʹ��Triton X-100��NP-40�Ⱦ���ϴ�Ӽ�����Ҳ����ʹ�����գ�����20����ػ����ա�ͬ����������ʩ�ӵ����ʣ���Ũ�Ⱥͷ���ʱ��ɻ�ø��ֽ���������Ӧ�ڿ�ʼʱ���Բ�ͬ�IJ��������͵�����ʾͨ��Ϊ0��
���Ҫͨ��IF����֬����ػ�Ĥ���ף���Ӧ��ϸ����ͨ���裨=֬��ȥ������Ϊ��Ŀ�ĵ�һ���ܺõ�ѡ�������أ�������ѡ���Եش���Ĥ��ȥ�����̴�����ʹϸ����Ĥ��������������ڿ���Ⱦɫ֮ǰû�������ã�ֻ��ͨ����ѧ�������̶�����ʵ�֣�������������Ա��ϸ������Ĥ��Ͽ�ԭ����������ϸ���ڿ�ԭ�⡣����DAPI��Hoechst�ĺ���Ⱦ�ϣ���μ�NucleusȾɫ����Ʒ�̶�������Ĥ������Ҫ����
�����ʹϸ����һ���ķ������Խ����С������Ҫ���衣Ϊ�ˣ�����ʹ��ţѪ����ף�BSA�����̷ۻ�Ѫ���еĵ����ʡ���Ҫ���ǣ���Щ��ϵ��ײ�����Դ��һ��������������֣�������������һ������������Խ���ɥʧ�����ʹ�ö�����������ɽ���в����Ŀ���һ���Ŀ��壬��ô����ķ�ռ���������ɽ��Ѫ�塣�����Һ��Ũ��ͨ��Ϊ1������ۣ�BSA����5��������Ѫ�壩������ϴ�ӻ���Һ��ϡ�͡������������½���30-60���ӡ�
ͨ���̶������ͷ���Ʊ���Ʒ�ͻᷢ��ʵ�ʵ����߷�Ӧ�����ڽ���Ʒ��������һ��һ��������Ա������İб�ṹ�����Խ�����һ��ͬʱӦ������Ʒ����������������һ���������Լ�Ӷ�ɫIF�еIJ�ͬ���֡����ȸ��������̣�����ѡ�ķ����Һ�н��п���ϡ�͡��������Ⱦɫ�����⣬����������δ�ṩ�й���Чϡ�͵��κ���Ϣ����Ӧ������1:50��1��1,000֮�����Ũ����ȡ���ڿ��������������ʱ����Ա仯��������Ĭ�Ϸ���ʱ��Ϊ1-2Сʱ��
���������ֱ����Ƶ������������ֱ�Ӽ���������Ʒ��װ����Ϊһ���Ѿ��������Լ���ӫ��Ⱦ�ϡ������ڼ��IF�У�����ӫ����һ��������Ĺؼ�������һ��������Ҫ���д���ϴ�ӣ��Լ��ٶ����ķ������Խ�ϡ��ڶ�����Ҳ�����ڷ����Һ��ϴ�ӻ���Һ��ϡ�͡����������û���ر�˵�����������1��200��ϡ�Ͷȿ�ʼ�����������·���1Сʱ���б�Ҫ�ںڰ��н��з������裬�Է�ֹӫ��Ⱦ��Ư�ס�
���߷�Ӧ��ͨ������DNAȾ�϶�ϸ����Ⱦɫ��һ���棬��ʹ�о���Ա����Ȥ�Ļ�����������������ڼ���ϸ������֯�����ڸ��õض�����һ���棬��ָʾϸ��״̬��������˿���ѣ���Ϊ�ˣ���ʹû��������Ҳ�ɲ���DNA��Ⱦ�ϣ�����Hoechst��DAPI����ˣ���Ӧ�÷dz�С�ģ�����Ƥ��ֱ�ӽӴ���ЩȾ�ϣ�������������PBS��ϡ�͵�Hoechst��DAPI���мĺ�Ⱦɫ10���ӡ�
���IF������밲װ��Ʒ���ʺ�������顣Ϊ�ˣ�ʹ�ù̶����ʣ�����Mowiol��Prolong Gold�����ù̶����ʽ���Ʒ�̶��������ز�Ƭ�ϣ����һ����Է�ֹ����ˮ�����⣬�̶����ʻ����������ʣ�����ڴ��ͽ��ᄉ����������������ġ�һЩ�������ṩ�˴������Ӽ��Ĺ̶����ʣ�����DABCO��һ�ַ���ɫ�����ɱ�����Ʒ���ڹ�Ư�ס�����ʹ�õ�ӫ��Ⱦ�ϣ�ijЩ����ɫ������������ɫ������Ч�����⣬������ʹ��������DNAȾ�ϵĹ̶����ʣ��Ա��ڰ�������ж�ϸ���˽���Ⱦɫ����������ϸ����Ⱦɫ�Ƕ���ġ����ͨ��ʹ��Ӳ���İ�װ���ʣ���Ʒ������ҹ�̻�����˵ڶ�����Խ���������顣�����ַ�ʽ�����������Ƽ��������������»�4��C�ĺڰ������ش��棬�������ס��ӫ��Ⱦ�ϵ�ӫ��ǿ�Ȼ�����ʱ������ƶ�������
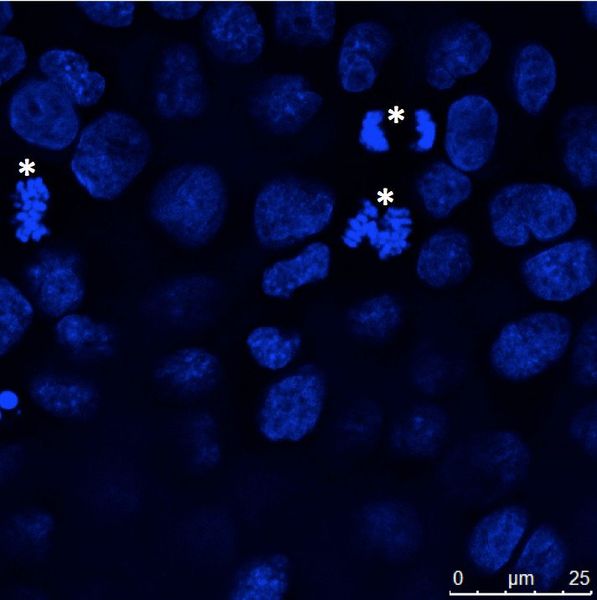
ͼ4��ճ����������Ƥϸ����MDCK�������ڸDz�Ƭ�ϣ��̶����ϸ������Hoechst 33342Ⱦɫ�������ϸ����ʾ����DNAȾɫ������Щϸ����ʾŨ����Ⱦɫ�壬����˿�����з��루�Ǻţ���������Leica TCS SP2�Ͻ��С�
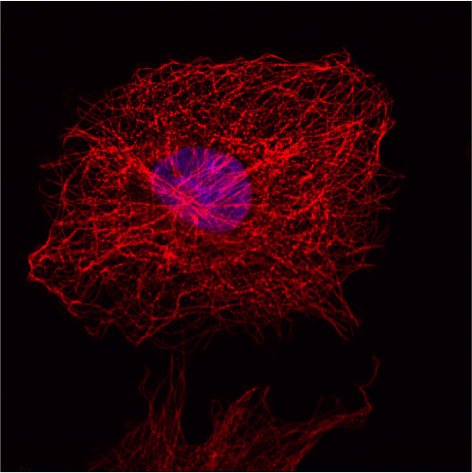
ͼ5����ͼ����ʾ�˳���άϸ����COS-7����ϸ��������ļ��IFȾɫ��ϸ������Hoechst 33342Ⱦɫ������Leica TCS SP2�Ͻ���������顣
����ӫ��ز����ٵ����ʵ����ƣ�����ȷ��������ͼ�ؼ�ȱʧ����ȷͨ���ᵼ�´���Ŀ϶������ʹ�������ݡ����ȣ���Ӧ�÷������̶������ͷ�յ���Ʒ���Ա��˽�ϸ�����ҵ��Է�ӫ�⡣��ʱ����ʹû��IFȾɫ���ṹҲ����ָ�ӫ���ԡ�
��Ϊ��һ���Ŀ��ƺ͵������IF������������ʹ�õ���ƷҲ�Ѿ��������������˴�����������ڶ�������������ȣ��⽫��ʾ������걾֮���ǿ�������Խ�ϡ���Σ����������������Ա��ڻ�ȡ�˿ؼ���ͼ���ڼ䲻��¼�κ��źš����������������ɼ�����ֵ�����ų����������ļ������źš���ֱ����Ƶ�У��Է�ӫ��������ڵ�����ֵ����������������������һ��һ���������Ʒ���ڼ��IF������������һ�������
Ϊ��ȷ����һ���������Եر������Ľṹ��һЩ�������ṩ�����ڵ�һ����ķ���ģ����Ŀ��ڸ��ض���ԭ���Ӷ���ֹ���������λ��ϡ���Ƚϰ���Ҳ��ȷ�����������Բ���˻�ÿɿ��������ѷ������ڶ�ɫIFʵ���У���������ע����ѡӫ��Ⱦ��֮��Ĵ��š�������״�ִ�ж�ɫIF�������ڵ������������������Ŀ��ṹ����Ⱦɫ��������Щͼ�����ɫͼ����бȽϡ����գ���Ӧ�þ���ϸ��ز鿴����ȡ�����ݣ�����������������ֵ����ͬһ��������������ݽ��бȽϡ�
| ���� | ��Ʒ�Ʊ� | ��...���� |
| �Է�ӫ�� |
| ϸ���Է�ӫ��ķ����� ֱ����Ƶ��������ֵ�� |
| �����������IF�� |
| �����ķ������Խ�ϡ� �����Ƶ��������ֵ�� |
| ��ɫIF |
| �Ƚϵ���Ⱦɫ���ɫͼ��
|
| ����� |
| ����һ���������λ�Ľ�������ԡ� |
��ǩ3��Ҫ�����ĸ��ؼ���
��ǰ������IF���������ŵ㣬��Ҳ��һЩȱ�㡣�ؼ�����Ʒ�Ĺ̶����̶���ζ��ɱ������˲��ٿ��ܽ��л�ϸ������̬���̵ķ�����˺ܸ��ӣ���Ϊ������ÿ��ʱ���̶���Ⱦɫϸ������ˣ�IF���۲쵽���ٵĶ�̬���̡�����Ȼ�DZ������ӫ���ǩ������GFP�����ںϵ������ƣ������ڻ�ϸ����������������IF���̣��̶�/ͨ�����ı��˷�����ϵ�ṹ�����α����ܻᱻ����Ϊ�������źš���ˣ�����Ϊÿ��IFȾɫ���ʵ��Ķ��գ�����ܺܺ�ʱ����һ��ȱ���Dz��ɱ���ģ�ӫ��Ⱦ�ϵĹ�Ư�ס�ӫ�⵰�ף���GFP��Ҳ�ܴ�Ӱ�죬�����ʵ������´洢ʱ����ʹ�������Ƽ��з�������Ҳ�ɼ�GFP���෴��IFӫ��Ⱦ��ʧȥǿ�ȵ��ٶȸ��죬������������������Ʒ�Ŀ���Ư��ӳ�˳������������п���ɫ���İ�װ����Ҳֻ���ڴ���ʱ�ṩ������
ͼ6��������������ͼ
��Ƶ����ij���ʱ�䣺Լ5��Сʱ��
����ͨ����ѧ�������̶�������ϸ���ڸDz�Ƭ�ϼ��IF�ı�������
����ʪ�ҷdz��ʺ�IF�����ҿ��Ժ��������ƣ���μ��õ�Ƭ���������ʪ�ҡ���������ֹ���Ƽ��ĸ���������ںڰ��з���������ڴ���ӫ��Ⱦ�Ϻ���Ҫ�������Ѿ����ڵ�ӫ�⵰���DZ���ġ�
��ѡ������Ҫʹ�Dz�Ƭ��ȫ��ʪ��ȷ����Ʒ��Զ������ȫ���
�����з���������������½��С�
��ϴϸ�����Σ��������ӽ��������Ϸ�תϸ���ĸDz�ƬС�ĵط����ʪ���С�
��4����ȩ��10���ӣ�Ȼ��ϴ��3�Ρ�
��0.1��TX-100 / PBS��15�C20���ӣ���ϴ��3�Ρ�
��5������ɽ��Ѫ��/ PBS��1��BSA / PBS���45���ӣ�������ϴ����
�ڷ����Һ��ϡ��һ����������Ӧ��2Сʱ������4��C��ҹ����������ϴ4���Գ�ȥδ��ϵ�һ����
���������1Сʱ���ڷ����Һ��ϴ�ӻ���Һ��ϡ�͡�
���������������Ҫ����Hoechst��DAPI [1 ��g / mL]��PBS�з���10���ӡ�������ϴ4������ʹû�к�Ⱦ��
����������ȡ�¸Dz�Ƭ���������dH 2 O�У��Գ�ȥϴ�ӻ���Һ�еIJ����η֡�
�������ز�Ƭ�ϵ�һ�ΰ�װ���ʣ�Ȼ�Dz�Ƭ���ã�ʹϸ�����á����������ᰴѹ��Ʒ��ʹ��װ���ʷֲ����ȣ������ἷѹ��Ʒ��
�̻�������������顣

1.Ҫ��װ��ʪ�ң�����Ҫ������Ʒ���������ϺУ���ĭ������Ƕ�һƬʯ��Ĥ����ʵ��ֽ����ˮ�����ӣ����ڴ����Dz�Ƭ��

2.��Ƕ���������У�������Ūʪ��

3.�����Ĥ����Ƕ���ϡ�

4.������С�ĵؽ��Dz�Ƭ�ӷ��Ĥ���̵����������Ƴ������Ƴ�ϸ������ǸDz�Ƭ��λ�ã���ȷ��ϸ����Զ�����dry��

5.Ūʪֽ������������ط��ں����ϡ�ע��ë����Ҫ�����Dz�Ƭ��

6.�����Ӹ��ں��Ӻ�ë���ϣ���ϸ�����������ʱ�䡣
�õ�Ƭ���������ʪ�ҡ�
��1��PBS�������λ���Һ��
��137���ף�NaCl
��2.7���ף�KCl
��10���ף�Na HPO 4
��1.8���ף�KH 2 PO 4
����HCl��pH������7.2�C7.4
������PBS ++��������Ũ��Ϊ1 mM CaCl 2��MgCl 2
������PBS-T������0.05��Tween����Ũ��20
����ȩ��
����4��PFA����ۼ�ȩ������pH 8����ů�ģ�50-70��C��dH 2 O�У���NaOH���ڣ���
������10��PBS����Ũ��Ϊ1��PBS������900 mL 4��PFA / dH 2 O�е�100 mL 10��PBS����
����HCl��pH������7.2�C7.4��
���״���Ԥ�����C20��C����
��100���״����C20��C��
���״�/��ͪ��Ԥ�����C20��C����
��50���״����C20��C����50����ͪ���C20��C��
��TX-100��Triton X-100����
����Ũ��Ϊ0.1��TX-100��PBS
�����أ�
����Ũ��Ϊ0.1�����յ�PBS
������ȥ�ۼ���������ͬŨ����PBS��ʹ�á�
��BSA��ţѪ����ף���
������Ũ��Ϊ1��BSA��PBS
��ţ�̷ۣ�
����Ũ��Ϊ1���̷۵�PBS
������Ѫ�壺
����Ũ��Ϊ5������Ѫ���PBS
��Hoechst��DAPI��
������Hoechst 33342��DAPI��PBS�е����չ���Ũ��Ϊ1 ��g / mL����Һ��
