

��ѧ�����������ԷŴ�С�����壬�Ŵ�Զ���ĺ��ǣ�����ʾ���ۿ�������ϸ�ڡ�����������֪��������һ�����˵����⣺�������ޡ����ǵ���������ѧ����������Ҳ��ͬ�������⣬�������źŵ�������ʶ����֪֮ǰ�����ǵĴ��Ի������ɾ������δ�۽�����Ϣ�����ͼ��������Ƭ�ϣ�����ʹ�á�ͨ���Ż����������ǿ������ӽ������ȣ��������ͨ���ᶪʧ�ֱ����Լ�zλ�õ���Ϣ��
�������ֻ��¼�۽���������������Ե�zλ�ã�����Խ���۽�������⣺�ڼ�¼һ��ͼ������ǿ����ؽ�����������û��ģ���IJ��ֲ�������������������ά�ȡ�
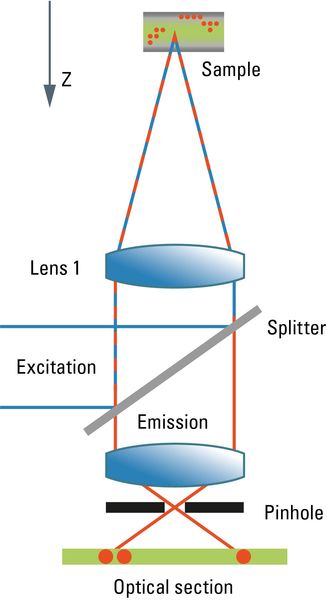
ͼ1�������Ĺ��۽�ɨ�������еĹ�·ʾ��ͼ�������⣨��ɫ��ͨ���������������ķֹ⾵��ϵ������У���ͨ���ᄉ1�۽������伫�㡣�����ͨ���ֹ⾵��������пռ��˲�����x��y������ɨ��������ͼ����ѧ���֡�
������ǣ������й��۽��������ἰ��ѧ��Ƭʱ���μǡ����۽�ԭ����ؼ��ɵ�����ѧ�����У����ܼ���������Ҫ���кܶ��ģ�������ͨ�Ĺ�ѧ������ͬ�������Ĺ��۽�������Ҫ�Ե�����߽��о�����С����������ߵ�ֱ���ɲ���ѧ���ƣ�����d�֦�/ NA���ﵽ���伫����Сֵ����ϸ��ǿ�ȷֲ��ɵ���չ����������ͬʱ�������������в⾡����С�İߵ㡣���ڹ�·�ǶԳƵģ������ͬ����ѧ���������ڵ�״������ĸв�ֲ���ͨ����������뵽���·���е��м���ƽ������ʵ�ֵ��������������������ͼ��Ľ�������غ�-��˲��á����۽�����������ͼ1��ʾ������������ǹ�ѧȥ�������в��Ǵӽ�ƽ�淢���Ĺ��ߡ����Ĺ�����z�����ϵĿռ��˲�����
���ڹ�ѧ��һ��ֻ����һ�����Ϲ�������˸õ������ϵ��³����ƶ���������ͼ��ǿ�ȱ�ͬ��ת��Ϊ������Ϣ�����洢�ڼ�����ϵ�֡�洢�С��Ӹõ��Ӵ洢���У�ͼ����ʾ����ͨ�������ϡ����ڱ������˳����ͼ�����ֻ����ijЩӰ��֡��ʽ�Ϳɽ��ܵ�����ȵ������£��ſ���ʵ�ָ�֡���ʡ��߶����Ĺ�·������LeicaSP������Լ��dz���Ч�Ĵ������������ϼ������HyDs������������߸�֡�����ܡ�ͬʱ�����۽�������ʵ�ָߴ�12,000 Hz����Ƶ����PAL�����ӵ���ƵԼΪ15,000 Hz�����ʵ��������£�֡������߿ɴ�ÿ��500���ǿ��ܵġ�������ˣ�Ϊ�˻�ȡ�㹻�ߵ������ͼ��֡����ͨ�����ᳬ��ÿ��10֡��
��ɨ������йص���һ�������ǣ���ƽ���Ϸ����·�����Ʒ����ᱩ¶�ڴ������������������ͼ��û�а����������ܵ���ӫ��Ⱦ�ϵĹ��������⡣����ӫ��Ⱦ��Ҳ���ڽ�ƽ���Ϸ����չ⣬��˵�������Ʒʱ��ӫ��ǿ�Ȼ�Խ��Խ���������ͨ���Զ��������������������Ҫ�������Ϊ���ۡ�
�����Ĺ��۽�����Ļ��������Ǹ߷ֱ��ʣ�����ʹ�ø�NA������ͼ���ڽ�ƽ���ڹ��еؾ��Ȳ���ʹ�ù��۽������������ɣ����ɵط������Ƽ�����ʵ�����۽��������ڱ���ͬ���ѧ����������ʦ��ͨ��һ���Ŀ��ؼ��ɷ������б����������ͶԱ�ģʽ����Ҳ���������͵�ɨ�������Ļ������������Ӽ������ߴ�г��������������ɿ�˹�п�˹����ɢ�������ͳ��ֱ��ʼ���STED���������������������
���ܹ��۽������ǹ�ѧ��Ƭ�Ļƽ�������������ǰ�ų����˵�һִ̨�д�������������� Spalt-Ultramikroskop��ʹ�þ۽��������Ȧ�е�������Դ������ƻ�̫�������ڶ�������ͨ���ǿ��ظ�ʹ�õ��ᄉ���������촹ֱ�������Ĺ���Ͷ�䵽�����С����������Ч�ش����˴�Լ�����Ƭ״�����������Ӧ�ó����漰�Ƿֱ������ӣ�������ɫ�����з�ɢ�Ľ���ʵ֤�����������ڸ��ֽ�����Ʒ�ͻ��ǽ��ʣ��ڻ�ѧ��ҽѧ�о���ͨ���������з������������ڵĹ�Ƭ���������ڹ۲����5����С��������ᵼ������������ɢ�䣬����ɢ���������Ĵ�ֱ����·���п���Ϊ����ͼ�۲쵽����Ϊ����������ӻ��˳�Ϊ�� Ultramikronen���IJ��ɷֱ�����ӣ���Щ���ӡ������������ķֱ��ʡ������������������������Ͱ�ʾ�˳��ֱ�����Ƶ����ͣ���������ȷָ������������Ȼ�ܵ���ѧ��������ơ�
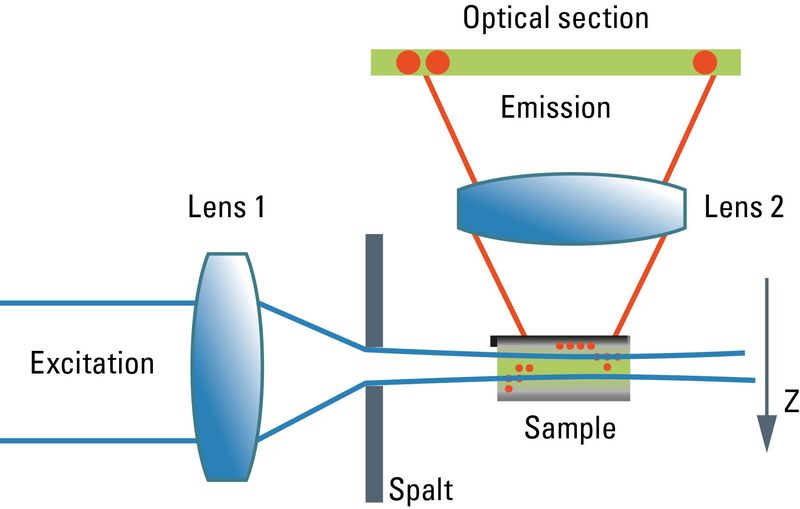
ͼ2��Spalt-Ultramikroskop�й�·��ʾ��ͼ�����������ᄉ1ͨ�����죨Spalt�������۽�����Ʒ�С��÷������ᄉ2�ռ����ҿ������������¼Ϊ��ѧ���֡�
�������������ƹ������������ƣ���������Ͳ������������ֱ�ڹ���Ĺ�Ƭ��Ȼ�����ֲ�������ӫ��̶���Ʒ����ʵ֤���������������ں���Ʒ�Ŀ���ʵʱ�����ر���������ΪƯ�ײ���ô���ԣ�����������������۽������ֱ��������ִ��ͼ���¼����Huisken��ʾ����z�����ϵ����ղ������⣬��Ϊ����ʦ���ھ۽���zλ���ϵ�����λ�õ��նȾ���ȡ����ǣ�������������ͨ����һ��ͨ����Ʒ������ܻ�ʹ����Ʒ�е�ͼ����ij�̶ֳ����ӻ�����Ȼ�ں���������ӰЧ���������������������Ʒ��һ�����չ⣬���ӫ�����෴��һ��䰵��Voieͨ����ת�������ռ���ͬ�����ͼ������������Ӱ�졣Dodt��������ԵIJ�����������Ʒ���Բ�����Ƭ�����ա����գ�Keller������ʹ��ͶӰ�����������������ɨ���˴�ֱ�ڹ۲����ϸ���������÷�����Ϊ������ɨ���Ƭ����
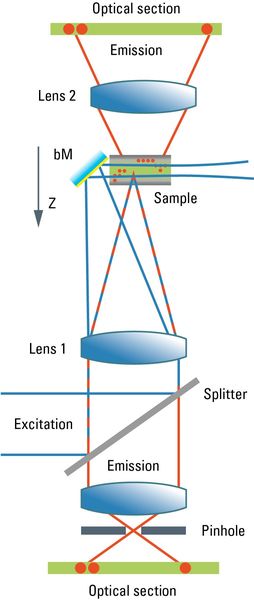
ͼ3�������Ĺ���ɨ��ʹ�ֱת�����ֹ�Ƭɨ�������ںϹ�·ʾ��ͼ���й���ϸ��Ϣ����μ�ͼ1��2��ͼ�������������������ֹ�ѧ��Ƭģʽ֮�����л���
���ַ���������������ҽѧ�о��ͳ����о��У�Ϊ����ѧ����ͼ����Լ�ϸ���ɷֵĹ��������ṩ�������µļ�������⡣���������棬���ַ�ʽ�кܴ�ͬ��������������Ϊϵͳ�Ķ������֣�����ͬ�����������ִ�������۽�����ʹ�ù���ɨ��ϵͳ������άͼ������ɨ��Ĺ�Ƭʹ�ù���ɨ���������������������������һ�����⣬���Ƿ��п��ܽ����ֲ��Խ����һ����һ��ϵͳ�С����ϵͳ��˾�������TCS SP8 DLS��������������Ϲ�Ƭ������
�TCS SP8 DLSͬ��ɨ���豸������ͨ�Ĺ��۽���������ͬ��ɨ���豸ͨ�������������ڿռ��Ϲ���ɢ������ִ�й�ѧ��Ƭ��ͼ��ͨ������ɨ�辵���������������ƶ�������������ɡ�Ҫ��������ϵͳת�������ֹ�Ƭ����������ʹ����������ֱ�ڹ��ᴩ����Ʒ��ͨ���ڽ�ƽ���λ�ô����ڹ۲쳡����������һ��С���ӣ�����ʵ�����������������������ƫת����۲쾵��е���ӣ���ȷ��������zλ��ʼ�մ���ͼ�����ɹ�ѧϵͳ�Ľ����ϣ�
���������ĵ���λ�ò��������άͼ��ֻ�����һ��ֱ�ߡ����������ڹ��۽������й���ʵ�ֵĺ���ɨ��ģʽ֮һ���ڴ�ֱ������ɨ�������ߣ��Ӷ���������Ķ�άƽ�档
������෴��һ�����ڶ������侵����ֻ��ʹ�ù��۽������Ĺ���ɨ��װ�õĵڶ��ᣬ�Ϳ���ͨ��ͬһ��������������Ʒ���������˲��������������Ӱ����Ҫ��Ȼ���ٴδӾ��в�ͬ�������������ͼ��������ͼ��
Ϊ���Թ���ģʽ����z�����������붨λ��ʹ���������Ľ�����Ҫ����������غϡ�Ȼ��ɨ����̽������ӳ����ڲ������Dz������۽������ij��÷�����Ҫ�л�����Ƭ�ɼ������뽫�����ƶ���Լ���ӵ�����ľ��롣����������£�����������ƽ��������ֽ�����۲쳡�����ġ�ɨ���豸��Ҫָ����Ұ�ı�Ե����ײ�����ӡ�
������ϲ������Խ����ֲ�ͬ�������ϲ�Ϊһ���������Ӷ������������ɱ������һ����Խ�����Ĺ������������ֹ�Ƭ�������ϡ���ˣ�ͬһϵͳ����ʹ�����ʺϽ����ǰ�о�����ļ�����̽���κ���Ʒ�����ڹ���·�������ڹ�����Լ������յ�Ч�������Ƭ������������ṩ�˸����µ�Ӧ�û��ᡣ
