

- 您好,欢迎您访问成贯仪器官方网站!


在任何搜索引擎中输入“荧光的定义”这个短语,你会得到如下的短语或者类似的东西;
“由于较短波长的入射辐射如X射线或紫外线,某些物质发出的可见或不可见辐射。”
这个定义如何与荧光显微镜相关(图1)?“较短波长的入射辐射”仅仅是用于“激发”样品中荧光团的光源。这种光可以包括可见光谱,紫外线(UV)和红外线(IR),显微镜中的光源可以从汞灯或氙弧灯到激光器。所述的荧光团(“某些物质”在上述的定义)是具有特殊性能,由此它们可以由具有较低波长的光激发后再发射更高波长的光/光子的化学化合物。
波长的基本单位是仪表,“波长”定义为光波的两个连续波峰或波谷之间的距离。波长的符号是希腊字母lambda(l)。通常在显微镜中使用的波长在400-700nm之间的可见光谱内,400nm以下的UV光谱和在700nm开始的IR光谱(图2)处于纳米(nm)范围内。

荧光团按其激发和发射波长分类,通常以显示最大峰值的图形的形式进行分类。荧光基团在所谓的“基态”中是天然稳定的。当它们吸收光子(来自“较短波长”光)时,光子的能量将荧光团的电子升高到更高能量的“激发”状态。被激发的电子不会保持在这种状态,但是在返回到基态时会失去振动能量并发出更长波长的光子。对于显微镜中使用的荧光团,从激发到返回到地的一个完整周期占据0.5到20纳秒的区域。
荧光团激发和发射波长通常缩写为带有下标“ex”(激发)或“em”(发射; l ex或l em)的希腊字母lambda 。
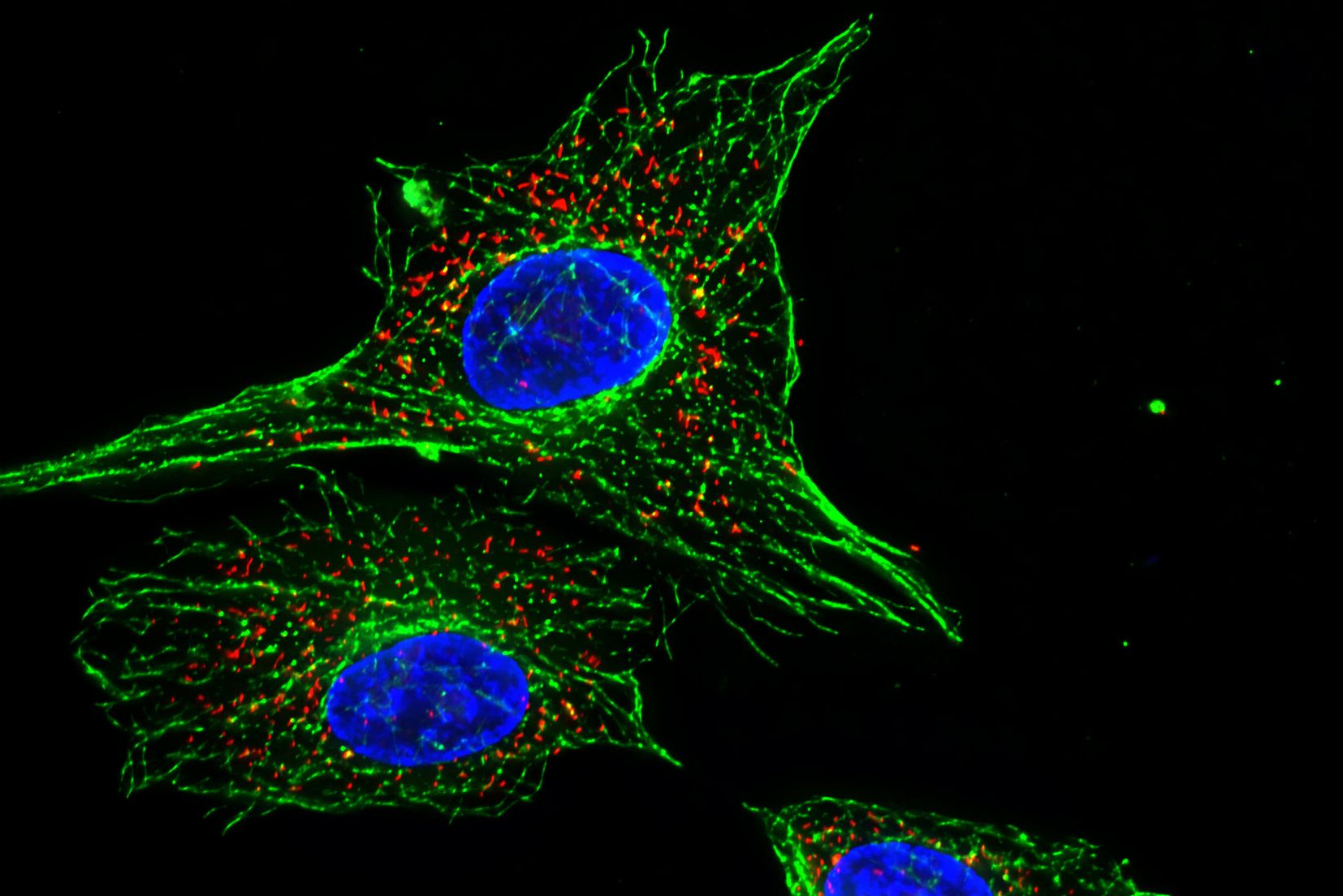
每个荧光团都具有不同的最大激发和发射光谱,并且该属性用于区分同一标本中的不同物镜。例如,使用荧光染料DAPI(4',6-二脒基-2-苯基吲哚)突出显示细胞内的核蛋白以及荧光标记的鬼笔环肽以突出显示肌动蛋白细胞骨架。
波兰物理学家亚历山大・贾布朗斯基教授(Aleksander Jablonski,1898-1980年)是第一位在三层能量图中描述地面/激发/发射之间的循环的方法,该方法简单地称为“雅布隆斯基图”。1930年,他从华沙大学获得博士学位,题为“关于激发光波长变化对荧光光谱的影响”。1933年,他发表了他的论文(“染料中反斯托克斯荧光的效率”),其中载有Jablonski图。荧光团行为的这种简单但有效的说明突出显示了从基态到激发态的激发以及随着发射更长波长的光子而回到地面(图3)。
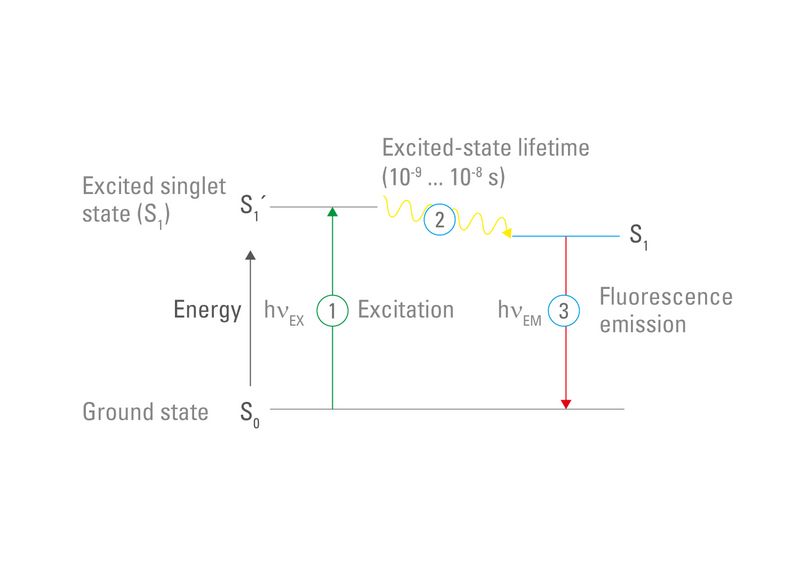
虽然图3是简化的Jablonski图,但应该注意的是荧光团可以存在于许多不同的激发和发射状态中。此外,取决于分子的电子自旋,荧光团可通过称为“三重态”的不同松弛状态返回地面。
乔治加布里埃尔斯托克斯爵士(1819-1903)是爱尔兰数学家和物理学家,在他一生中,他在光学和光学领域取得了许多发现和进展。他于1849年被任命为剑桥彭布罗克学院数学卢卡斯教授,直到1903年去世。他写了一篇精美的描述性文章,于1852年出版并被称为“关于光的可变性的变化”。本文中使用的语言与我们在现代科学文献中习惯的语言不同。以下是斯托克斯使用的精彩语言的两个简短摘录;
“在去年秋天结束时,当季节的迟到提供了很少的观察机会时,我从不同的来源获悉,已经被提及的具有如此高度的内部分散性的黄色玻璃是用铀氧化物着色。“
和:
“当插入到无形的光线中时,管子瞬间点亮了,这确实是一种奇怪的景象:它实际上是黑暗可见的,总而言之,这种现象具有某种神秘的外观。”
“斯托克斯位移”后来以他的名字命名。当激发的电子返回到基态并发射光子时,波长总是比用于激发荧光团的波长更长。这是由于光的特性,其中波长与辐射能成反比。斯托克斯位移描述峰值激发和荧光团的峰值发射波长(图4)之间的差值(单位为纳米)。
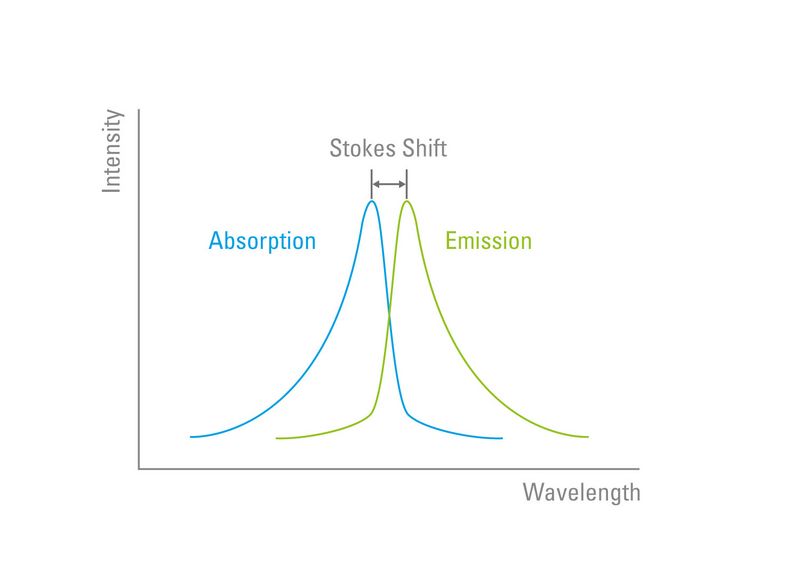
随着斯托克斯位移的增加,区分荧光团的激发和发射成比例地更容易。荧光团在它们的斯托克斯位移方面具有独特的特征,这是由于它们的电子构型和分子结构。
斯托克斯首先用“荧光”一词来形容他所观察到的现象,但历史可以追溯到1565年。西班牙的一位医生和植物学家尼古拉斯・蒙纳德斯描述了一种奇怪的蓝色,Lignum nephriticum。尽管有这些早期的观察,但在400年后的今天,在活的有机体中报道了绿色荧光物质。1955年,Davenport和Nicol发表了一篇论文,描述了称为Hydromedusae的水母亚类的嗜酸性粒细胞中的上皮组织。当时,这项工作的作者没有意识到嗜酸性粒细胞含有绿色荧光蛋白(GFP)。
直到1962年,Osamu Shimomura(* 1928)发表了一篇文章,其中上镜部分被认为是一种蛋白质。与他在普林斯顿大学的教授(弗兰克约翰逊)合作,他们从生物发光水母Aequorea victoria收集样品。他们有一种独特的方式从水母中分离荧光蛋白,即通过棉布袋挤压孤立的生物发光组织,生成一种下村被称为“挤压物”的解决方案。
1994年,哥伦比亚大学的Martin Chalfie(* 1947)教授编写了一篇论文,证明编码GFP的基因可在原核和真核细胞(即大肠杆菌和秀丽隐杆线虫的神经元)中功能性表达。该论文指出:“因为这种荧光不需要外源底物和辅因子,所以GFP的表达可以用来监测活体中的基因表达和蛋白定位。” 正是这份出版物为在生物学研究中广泛使用GFP铺平了道路。
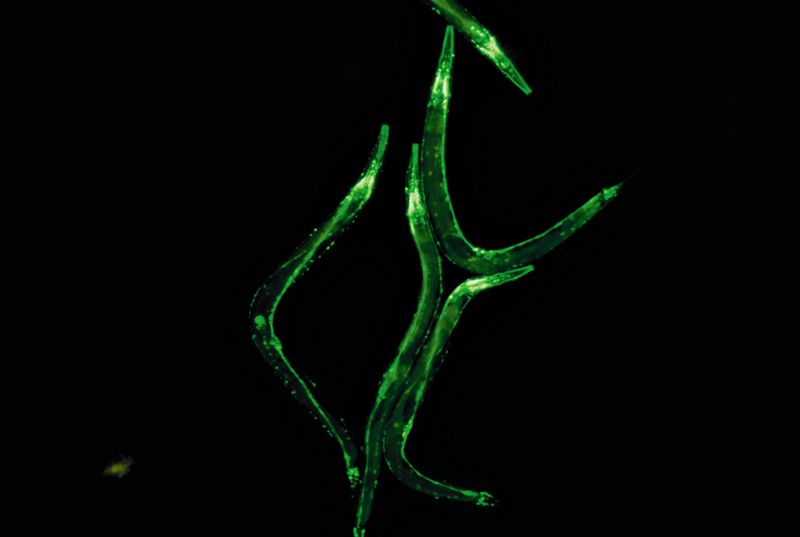
一年后,圣地亚哥Califronia大学的Roger Tsien教授(1952-2016)(他一直在研究野生型GFP的突变体)在自然界的科学通信中发表了他的研究成果Tsien及其同事选择了这种单点突变(S65T)的发现,因为它具有最长的激发和发射波长(490/510 nm),使其更具光稳定性,并导致众所周知的GFP激发/发射峰。
2008年,Shimomura,Tsien和Chalfie 因其角色和GFP的发现而共同获得诺贝尔化学奖。当Shimomura举办他的诺贝尔讲座时,他说:“当我在1979年发现GFP的发色团时,我认为我已经尽了我所能做的所有GFP,并决定终止我在GFP上的工作,以便集中精力研究生物发光”。他继续承认,“ GFP是一种美丽的蛋白质,但在发现后的30年内它仍然没有用。”
自从Tsien的发现以来,他的实验室设计了许多GFP变体,覆盖了大部分可见光谱,并且确实革新了光学显微镜和成像领域。由于这种基因工程,GFP的颜色范围从蓝色部分(EBFP; 380/460 nm)到黄色部分(YFP; 514/527 nm)。
与成像领域一样,荧光团可以用作“标记”来研究细胞和生物体中的基因表达。酶萤光素酶以及编码GFP的基因是通常用于检查特定基因是否由细胞表达的那些。用基因修饰的病毒DNA或表达靶基因时发荧光的质粒转染生物体或细胞。然后可以在转染的细胞中观察和检查细胞内的感兴趣的细胞器或部位。
用荧光团标记(或“标记”)的抗体通常称为“荧光探针”。在广泛使用GFP和发现之后的其他荧光团之前,用于标记抗体的两种最常用的荧光团是FITC(异硫氰酸荧光素)和TRITC(四甲基若丹明异硫氰酸酯)。尽管FITC和TRITC仍在使用,但在该领域取得了重大进展,荧光团和探针的选择至少是很广泛的。
当然,今天在实验室使用的最广泛的荧光团之一是“Alexa Fluor”染料。可用的Alexa Fluor染料的当前范围跨越可见光谱范围从346到784 nm的激发波长。
量子点(或“量子点”)在1981年由俄罗斯科学家阿列克谢・埃基莫夫在玻璃矩阵中首次发现,同时在圣彼得堡的瓦维洛夫州立眼科研究所工作。然而,Qdots的第一个胶体溶液是由路易斯布鲁斯发现的,他在新泽西州的AT&T贝尔实验室从事半导体工作。他现在是哥伦比亚大学化学教授。在1983年和1984年发表的两篇论文中,Brus描述Qdots为“小型半导体微晶”。
量子点表现出特殊的方式 - 尽管它们含有少至100到100,000个原子,但它们表现出的性质好像它们由单个原子组成一样。然而,它们确实符合荧光团的性质,从而它们可以吸收光能,变得激发并在返回到基态时释放光子光子。但是它们发射的光的波长取决于Q点的尺寸 - Q点越小,发射波长越短。这个属性是由于较小的Qdots拥有更大的“最小带隙”。这是激发电子到更高能态所需的能量。由于较小的量子点需要更多的激发能量,因此它们随后发射较低波长的光(波长与激发能成反比)。
几乎是20年后的2002年,Qdots成为加利福尼亚Quantum Dot Corporation的生命科学研究人员的商业化产品。
量子点是用于荧光应用的非常明亮和稳定的工具。研究表明,量子点比传统荧光团亮几个数量级,虽然它们与有机染料相比明亮多少有一些变化。就光稳定性而言,据报道量子点比传统荧光团稳定多达100倍,并且在一次体内成像研究中,它们仍保持荧光长达四个月。
在常规的荧光探针中,一个或多个荧光团可以连接到单个感兴趣的抗体上。然而,由于Qdots的表面积非常大,许多分子和抗体可以附着到单个点上,这可能具有许多优点,包括荧光信号放大。Qdots的使用还可以在多种测定中提供优势,其中多种波长可以同时成像。在这样的测定中,唯一的变量是由研究人员选择的Qdot的大小(以及因此的发射波长)。激发多种量子点可以与白光同时进行,这样可以抵消多个激光器的使用,并且可以进行许多调整以形成最终图像。