

- 您好,欢迎您访问成贯仪器官方网站!


TIRF显微镜的特殊功能是使用van逝场进行荧光团激发。与使用弧光灯,LED或激光的标准宽视野荧光照明程序不同,,逝场从盖玻片/介质界面开始仅穿透样品约100 nm。这允许从盖玻片开始以非常高的轴向分辨率对样本进行“附加”光学切片,并为特定应用带来了多个优势。
TIRF显微镜的一大优势是其出色的信噪比。由于the逝场的穿透深度低,离焦荧光最小,因此几乎没有背景荧光发生。因为只有一部分细胞暴露于电磁e逝波的能量,所以有害氧气的产生以及因此对细胞的光毒性应力也大大降低了。这极大地提高了细胞活力,并允许更长的实验时间。此外,低水平的光致漂白仅发生在电池的一小部分。由于有新的荧光团从胞质溶胶稳定流入该区域,因此信噪比在很长一段时间内保持恒定。除此之外,适用于TIRF显微镜(例如EGFP,Fluo-4等)的范围很广,并且仅受可用激光束的限制,因此可以轻松执行活细胞成像技术,例如FRET,FRAP和钙成像等。光敏相机的连接可实现高速图像采集,以观察快速事件。另外,TIRF显微镜可以与其他显微镜技术相结合,例如落射荧光显微镜和明场对比法。TIRF显微镜的缺点是,到目前为止,只有贴壁培养的细胞才能用于实验,例如,切片通常与盖玻片/培养基界面的距离不足以使van逝波穿透样品。
通过使用空间受限的渐逝场来激发荧光团,TIRF显微镜可以观察质膜附近(通常在100 nm附近)的光学区域中分子和过程的定位和动力学。这对于处理质膜中或质膜附近的许多应用是有利的。
TIRF显微镜是一种出色的技术,可将动力学研究与活样品甚至体外的空间信息相结合。它通常用于研究分子运输,例如在细胞骨架装配中发生的分子运输。TIRF显微镜中的快速图像采集和出色的背景消除为观察动态事件(如将蛋白募集到质膜)提供了极好的条件。因此,例如,可以研究动力蛋白/动力蛋白介导的运输的动力学。也可以使用TIRF显微镜跟踪整个细胞器(如线粒体)。为了研究细胞之间的相互作用,可以使用TIRF轻松查看特殊的结构,例如细胞的黏着斑显微镜观察,例如募集部分细胞骨架粘连。
通过将数学模型(例如质心跟踪方法)与无与伦比的信噪比和TIRF显微镜的z分辨率相结合,可以实现1纳米精度的单分子亚衍射极限定位。这是可能的,因为e逝波激发的荧光团产生了离焦荧光团的低背景荧光,从而导致在指定体积的样品中信噪比较低(例如the逝波的穿透深度)乘以视场面积)。在常规的基于灯的荧光系统中,光束路径中的所有荧光团同时被激发和检测,而没有关于其z位置的任何信息。
换句话说:荧光团的三维分布仅在二维中显示,因为细胞的不同z平面在获取的图像中显示为一个平面。这导致图像中的荧光团重叠,这通常使得无法区分单个荧光点。然而,在TIRF显微镜中,在大约100 nm深的e逝波中,只有相当数量的荧光团被激发,从而提供了样品的光学z截面。
由于从其他z平面发出的荧光团发出的光未覆盖检测到的信号,因此TIRF图像中x和y方向上的荧光点之间的空间邻近度相对较低。如果随后应用数学模型(例如质心跟踪方法)来计算检测到的荧光分子的质心,则单个分子的亚衍射极限定位可能会达到1 nm。
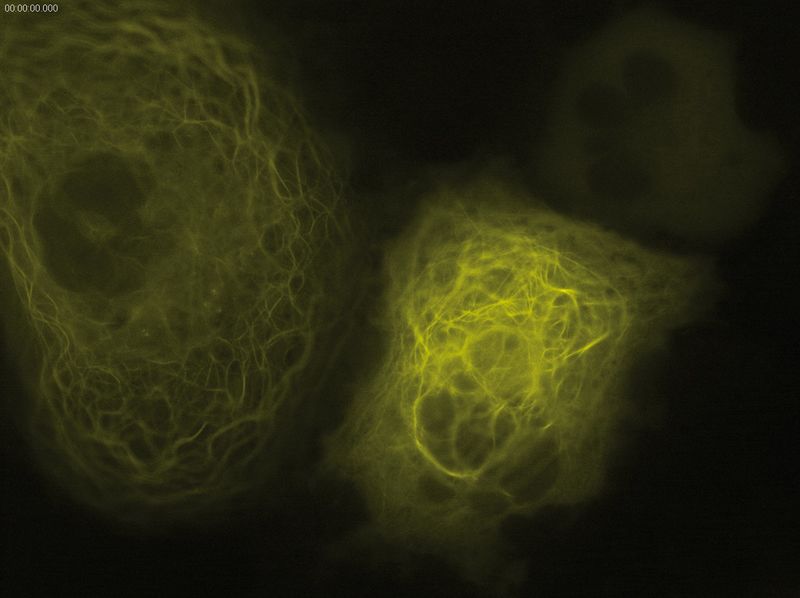
图1:表达YFP的微管蛋白的宽视野图像
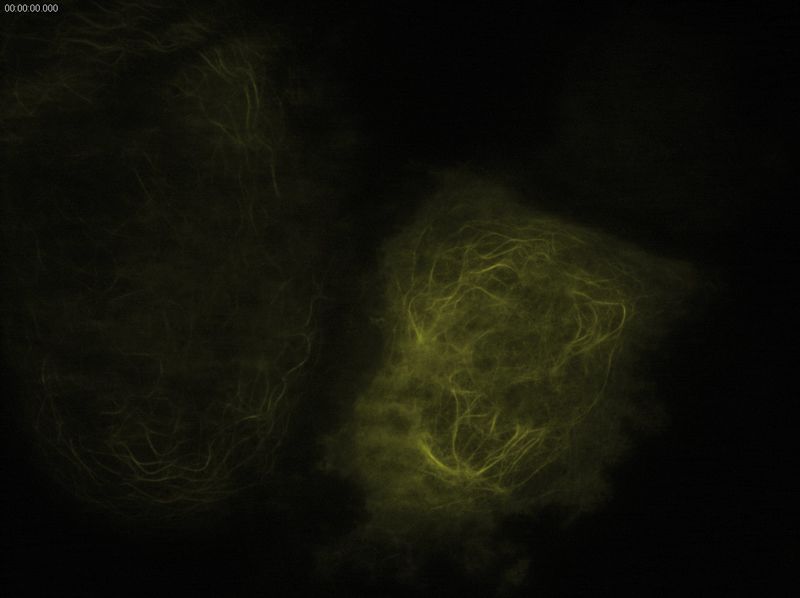
图2:微管,YFP的TIRF图像,穿透深度:120mm
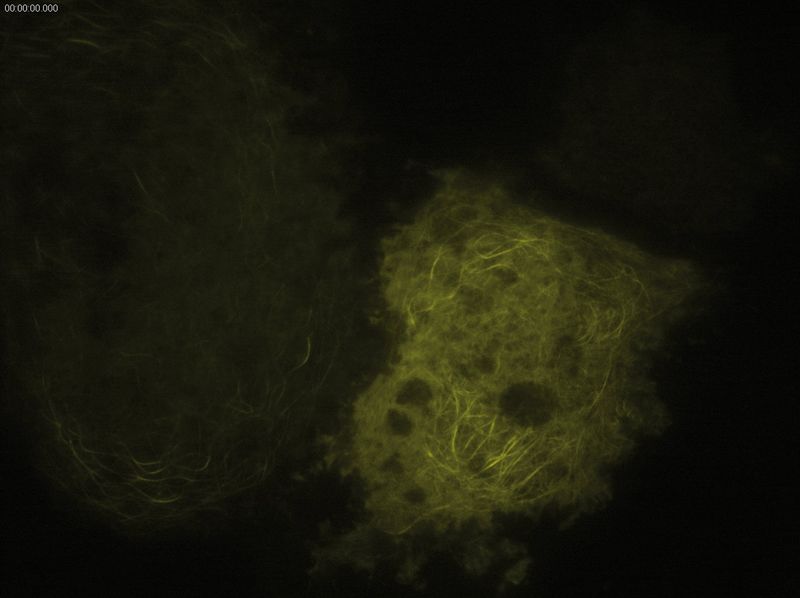
图3:微管的TIRF图像,YFP,穿透深度:90mm
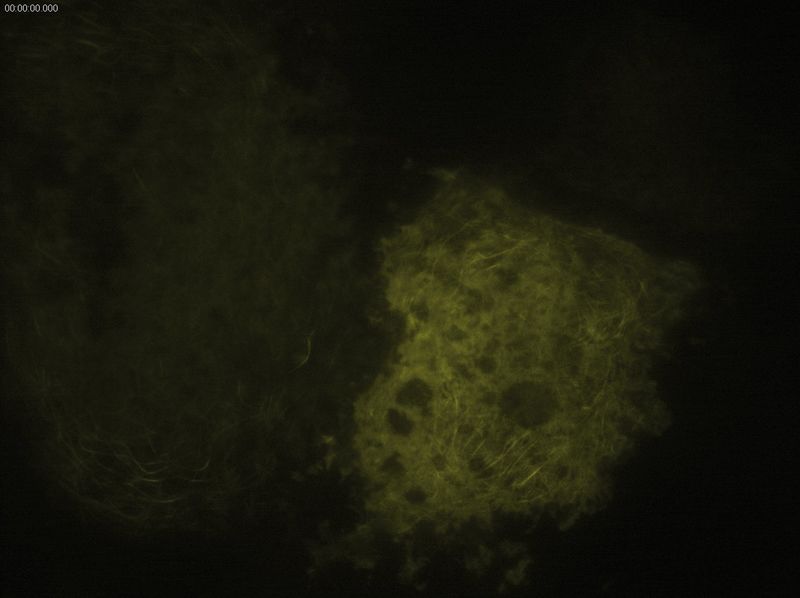
图4:微管,YFP的TIRF图像,穿透深度:70mm
TIRF显微镜的另一个大应用领域是检查膜融合过程,例如囊泡运输。由于逝波仅激发靠近质膜的荧光团,因此有可能监测内吞性囊泡的形成以及分泌性囊泡与质膜的融合。为此,可以通过用荧光蛋白(例如GFP)标记胞吐货物蛋白来标记囊泡。
由于光学切片,可以将荧光强度的变化解释为荧光标记的囊泡移入或移出渐逝场或货物释放或吸收。强度的相当缓慢的增加将暗示向消逝场的运动,并因此向质膜的运动。分泌囊泡与质膜融合后,荧光信号随着货物释放到细胞外空间而迅速下降。反之亦然,可以通过使用荧光底物(如标记的葡聚糖)观察内吞作用,该底物在细胞内吞过程中被细胞吸收。
在质膜上发生的另一个重要过程是细胞信号转导(例如,G蛋白偶联受体的信号转导)。在此,例如可以观察到信号级联中单个分子(例如G蛋白)的募集或移动。
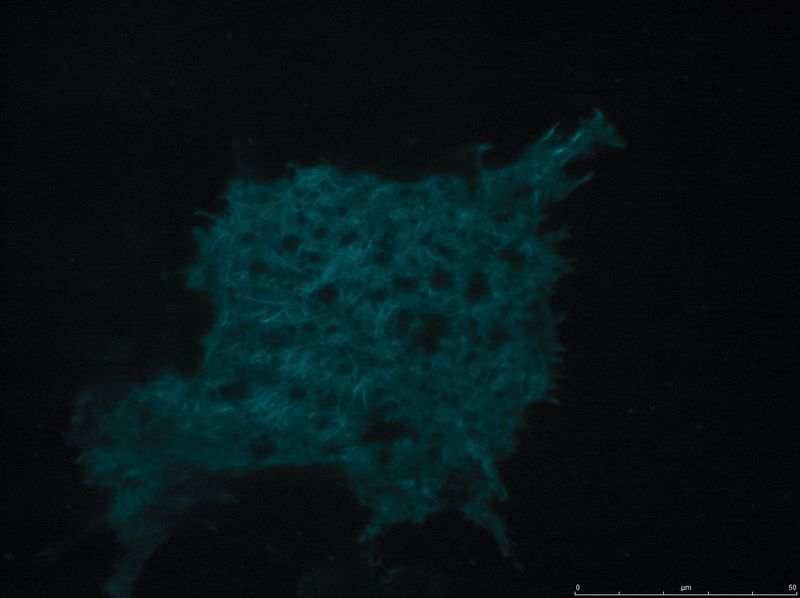
图5:YFP表达的Galectin3的宽视野图像
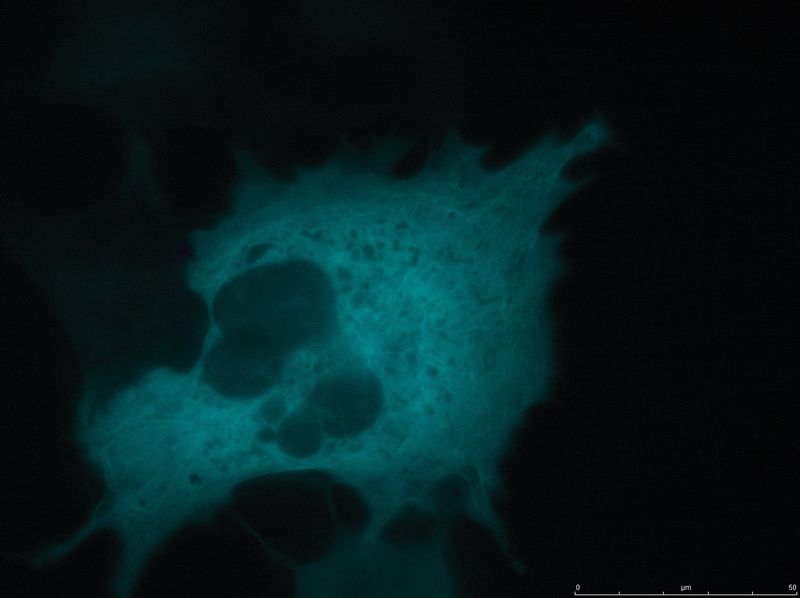
图6:Galectin3 YFP的TIRF图像
所有图片:图片由德国马尔堡大学临床细胞生物学和细胞病理学系马尔堡大学R. Jacob博士提供