

- 您好,欢迎您访问成贯仪器官方网站!


在慢性炎症过程中,某些身体部位会反复发炎。这伴随着许多人类疾病。借助宽视野光学显微镜,可以检查从细胞水平到整个生物体的潜在过程。本文介绍了几种宽视野显微镜应用,例如免疫荧光,活细胞成像,组织学和比率分析,以深入了解慢性炎症的发展,相关疾病及其治疗。
宽视野显微镜的特点是可以照亮整个标本,与共聚焦显微镜不同,共聚焦显微镜只能照亮一个小点。它的变体,特别是宽视野荧光显微镜,是生命科学中应用最广泛的技术之一。例如,对标本中各种荧光标记物(固定或活着)的检测可以洞悉许多生物过程,例如人体免疫系统。
人体在微生物入侵时会表现出先天性和适应性免疫反应。随着时间的推移,适应性反应会产生高度特异性的反应,而先天性反应会立即对病原体上发现的特殊结构起反应。它们被称为病原体相关分子模式(PAMP)。脂多糖(LPS)是革兰氏阴性细菌细胞壁特有的,是这种模式的典型例子。LPS与人类细胞表面的一种特殊受体结合,即toll样受体4(TLR4)。一旦结合,它就可以触发细胞内过程,最终产生促炎蛋白,称为细胞因子(图1)。
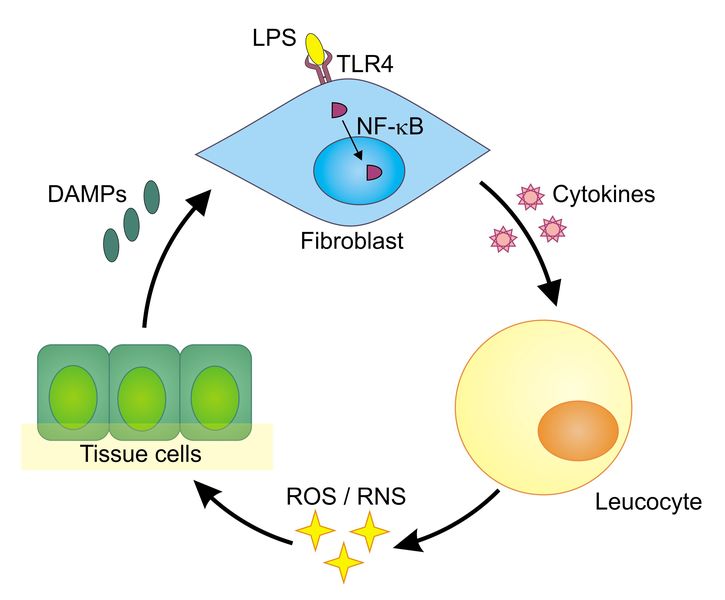
图1:toll样受体的自由基循环是慢性炎症的分子基础。一个起点可以是PAMP(例如革兰氏阴性细菌LPS)与成纤维细胞的结合。它们与TRR4等PRR结合,二聚化后会触发NF-κB易位进入细胞核。那里,NF-κB刺激促炎细胞因子的转录。这些细胞因子继而吸引产生ROS和RNS的白细胞(白细胞)。ROS / RNS杀死细菌和病毒,但附带损害也损害周围的组织细胞。DAMP可能由组织细胞的氧化磷脂产生。DAMP继而可以触发PRR(例如TLR4),从而关闭反馈和放大环路。除了刺激PRR外,还可以通过促炎性细胞因子(例如TNFα),ROS(例如H2O2),通过自由基诱导辐射和高迁移率的box-1蛋白(HMGB1)。在光学显微镜下可以观察到TLR自由基循环的许多方面。
该细胞内过程中的一个步骤是蛋白NF-κB从细胞质转移到细胞核中。NF-κB作为转录因子发挥作用,支持相关细胞因子基因的转录。此后产生的细胞因子促使白细胞(白细胞)释放可杀死细菌和病毒的活性氧(ROS)和活性氮(RNS)。不幸的是,ROS / RNS还会引起附带损害,并且可能对细胞本身产生负面影响。受ROS / RNS损伤的组织细胞释放出所谓的损伤相关分子模式(DAMP),它们本身可以触发TLR,从而再次启动整个过程并导致慢性炎症。
除了上述通过DAMPs进行的内在活化外,还可能存在其他过程中产生的物质开始循环的可能性。实例是促炎细胞因子,例如肿瘤坏死因子α(TNFα),ROS(例如通过进一步的细胞过程产生的H2O2)和自由基诱导辐射。
可以使用倒置研究显微镜来弄清炎症的分子过程。本文介绍了广角镜对我们团队的意义。最初,我们考虑购买共聚焦激光扫描显微镜。取而代之的是,出于实际原因选择了结合反卷积的宽视野荧光显微镜,例如,对于仅在有限时间段内加入该小组的学生的培训时间较短。此外,宽视野荧光显微镜具有非常好的活细胞成像能力,并施加了相对较低的光强度,从而降低了细胞压力。
配备了各种荧光激发块,专用物镜,快速滤光轮,气候控制和便捷的成像软件的宽视场显微镜可以为TLR自由基循环的许多方面提供照明。从普通的明场显微镜到免疫荧光实验,再到活细胞和FURA成像,我们可以研究重要的现象,例如动物患病组织的命运,LPS触发TLR4以及随后NF-κB易位至细胞核以及炎症后的Ca2+反应。
细胞培养。为了对NF-κB进行免疫荧光成像,使用了稳定转染了人TLR4,MD-2和CD14的HeLa细胞。根据制造商的说明,将细胞在补充有10%FCS(胎牛血清)和抗生素的DMEM(Dulbecco改良的Eagle培养基)中培养 。对于显微镜实验,将细胞接种在玻璃盖玻片上,并在达到60-80%融合时用于实验。
成像。所有图像均在配备Leica Application Suite X(LAS X)软件的Leica DMi8倒置显微镜上拍摄,该软件配有用于组织学样品的Leica DMC2900彩色相机和用于荧光成像的Hamamatsu Flash4 Cl sCMOS相机。为了进行活细胞实验,将孵育室连接至显微镜主体,以提供5%CO2和37°C的温度。使用嵌入在LAS X成像软件中的AutoQuant算法执行盲反卷积。
NF-κB的免疫荧光动力学。对于NF-κB易位测定,将接种在盖玻片上的细胞用50 ng / mL LPS刺激60分钟。刺激后,将细胞用PBS中的4%甲醛(1x;磷酸盐缓冲盐水;钙和镁; pH 7.0-7.2)固定。然后,使用一抗和Alexa Fluor568偶联的二抗对固定细胞进行RelA(也称为p65)(NF-κB的亚基)染色。为了鉴定核区域,将细胞用DAPI复染。为了可视化细胞骨架,Alexa Fluor 488 Phalloidin用于染色肌动蛋白丝。将样品包埋在ProLong Gold抗褪色剂中,并使用Leica HC PL APO CS2 63×/ 1.40油物镜成像。
用GFP -RelA 瞬时转染HeLa细胞。为了观察体内的NF-κB易位,使用电穿孔将HeLa细胞用GFP -RelA质粒瞬时转染。GFP -RelA是Warner Greene的礼物(Addgene质粒#23255)。电穿孔后,将细胞悬浮液转移到含有细胞培养基的玻璃底皿中。转染后二十四小时,在显微镜下使用Leica HC PL APO CS2 63×/ 1.40油物镜和2×2相机装箱对细胞进行检查。用TNF-α(10 ng / mL)刺激细胞后,每五分钟拍摄一次图像。
FURA成像。对于钙的测量,使用FURA-2AM(Sigma-Aldrich)。这种FURA-2衍生物(乙酰氧基甲基)具有膜渗透性,能够进行比例实验。将HeLa细胞与FURA-2AM(1μM)孵育30分钟。根据其钙的状态,FURA-2具有两个最大激发。含钙的FURA-2在340 nm处激发,游离的FURA-2在380 nm处激发。两种情况下的最大发射波长均为510 nm。对于比例实验,在340 nm和387 nm激发后测量荧光发射强度,方法是使用快速滤光轮进行。为了在340 nm处也获得最佳照明,使用了Leica HC PL FLUOTAR(340)20x / 0.80 OIL物镜,具有优化的低至340 nm的透射率。为了施加液体,使用了定制的微型分配器。图像采集和比率测量使用LAS X软件。FURA成像和活细胞成像实验是在定制的塑料标本架的帮助下进行的,该标本架是为方便标本更换而生产的。可以将在圆形盖玻片上生长的细胞拧入标本架的两半之间,并用液体覆盖(图2)。

图2:为获得适当的FURA成像性能,使用了定制的样品架。可以将带有细胞的圆形盖玻片安装到塑料底部支架(左)上。随后,将顶部冠状件(中部)与底部螺合在一起,以获得一个水密皿(右),该皿可以充满细胞培养基。有了它,可以任意更换盖玻片以观察大量不同的样本。
组织学。4周龄的C57BL / 6小鼠接受1.5%DSS(右旋糖酐硫酸钠)溶解于饮用水中10天。之后,处死动物,并收集部分结肠用于组织学检查。根据常规实验室方法,处理结肠样品并将其与组织包埋中心Leica EG1150一起包埋在石蜡中。使用Leica RM2255切片机和Leica HI1210水浴将石蜡块切成4μm薄片。然后,将切片置于显微镜载玻片上,并使用标准方案用苏木精和曙红(HE)染色。
HE切片在显微镜下用Leica HC PL Fluotar 20×/ 0.80油物镜检查。根据样品的大小,对每张幻灯片的对照成像10次单块扫描,对DSS处理的小鼠进行21次单块扫描,然后使用LAS X软件重新组装。图7显示了每种情况下2×2图像的摘录。所有动物实验均在美因兹大学转化免疫研究所的Schuppan博士实验室进行。按照德国和欧盟的法规,包括执行欧洲理事会指令2010/63 / EU的德国动物福利法,对小鼠进行饲养,处死和处死。
LPS刺激后,NF-κB易位至核。炎症是由信号连锁反应触发的过程,该信号连锁反应从模式识别受体(PRR)的激活开始(图1)。这些PRR之一是收费型受体4(TLR4)。在LPS结合后,TLR4复合物诱导细胞内信号网络,最终激活转录因子NF-κB。然后,转录因子从细胞质转运到细胞核,并促进促炎性细胞因子的表达。
NF-κB易位至细胞核的过程可以用荧光显微镜研究。为此,将稳定转染了TLR4构建体的HeLa细胞暴露于LPS 60分钟。固定后,对RelA(NF-κB的亚基)进行了免疫染色。作为对照,未刺激的细胞也被标记。
在非刺激细胞中,NF-κB(品红色)主要位于细胞质中(图3)。用LPS刺激60分钟后,NF-κB易位进入细胞核。通过一个细胞绘制NF-κB的强度分布图,可以确认非刺激细胞中最高量的NF-κB可以在细胞核周围成像。尽管如此,在细胞核内仍可检测到较低的NF-κB信号,这可能是由于来自细胞核上方和下方的NF-κB分子发出的聚焦光所致。用共聚焦显微镜获取薄的光学切片可以减少这种情况的发生。
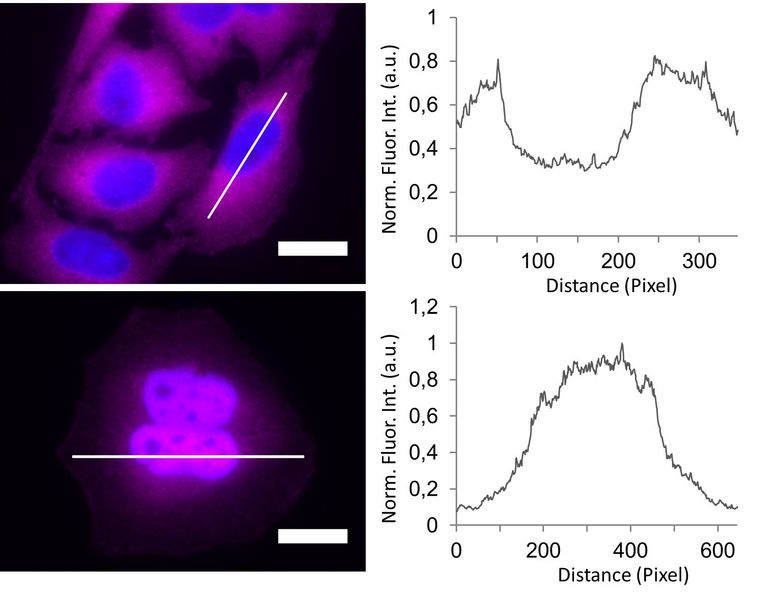
图3:在LPS存在下培养经TLR4转染的HeLa细胞。60分钟后,将细胞固定并免疫标记NF-κB(品红色)和细胞核(蓝色)。上排显示了未刺激的细胞,并根据白线绘制了相应的强度图。下一行描绘了LPS刺激的细胞,其强度图根据白线。LPS刺激60分钟后,NF-κB聚集在细胞核中。比例尺= 20μm。
反卷积是规避散焦光线造成的误解的另一种选择。宽视野显微镜不仅可以检测聚焦平面中的光,而且还可以检测例如来自其他区域的散射光。解卷积软件算法可以帮助将荧光信号重定向到其起源。图4显示了这种方法。用荧光显微镜对免疫染色的HeLa细胞进行成像,然后进行反卷积,该成像已集成在成像软件中。与原始图像相比,反卷积图像显示了更清晰的细节,同时仍保留了定量数据。因此,可以更精确地确定NF-κB分子的位置。
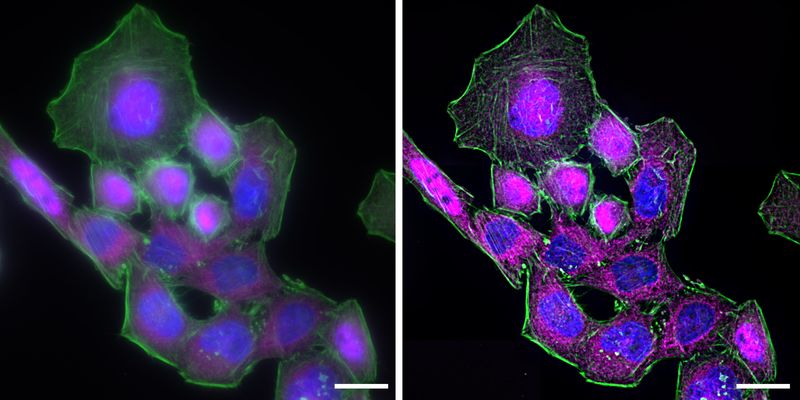
图4:用LPS刺激HeLa细胞,然后免疫标记NF-κB(品红色),肌动蛋白丝(绿色)和细胞核(蓝色)。反卷积有助于排除离焦信息。左图显示原始的宽视场图像,而右图则经过了反卷积处理。比例尺= 20μm。
可以想象通过在孵育后的不同时间固定细胞并测量细胞核与细胞质之间NF-κB的比例,将这些基于荧光显微镜的图像用作转运测定法。例如,在这种测定中,可以测试抗炎成分。可以将潜在的物质添加到细胞培养物中,并且可以直接观察其对NF-κB易位的影响。与其他基于筛选的方法相比,这将在单细胞水平上提供信息。
通过用荧光标记的蛋白质转染细胞,感兴趣的蛋白质的动力学也可以通过活细胞成像检测。为此目的,用NF-κB亚基RelA- GFP转染HeLa细胞。除脂多糖外,还有其他刺激可引起NF-κB易位进入细胞核。其中之一是TNFα。因此,在活细胞成像之前,已用TNFα处理了转染的HeLa细胞。
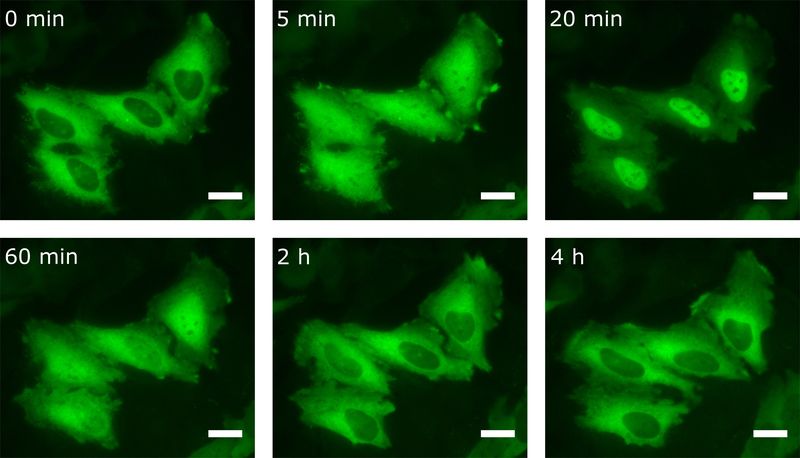
图5:HeLa细胞用NF-κB亚基GFP -RelA(绿色)转染,并在荧光显微镜下观察到。图像采集前五分钟,细胞被TNFα刺激,从而触发NF-κB易位进入细胞核。20分钟后,大部分NF-κB位于此处。随后,转录因子转位回到细胞质。比例尺= 20μm。
可以看到,TNFα刺激后,细胞核中的NF-κB浓度大大增加。20分钟后,大多数转录因子已经转移。有趣的是,在达到该峰值后,NF-κB开始重新定位到细胞质中。
建立上述荧光显微镜测定法以使用NF-κB作为炎症指示剂。它们可用于测试细胞培养系统中的促炎物质,尤其是抗炎物质。这可能会发现潜在的慢性炎症治疗方法。
炎症过程中的电信号传递。炎症反应与细胞内和细胞间电信号传导相关。离子通道与炎症高度相关,其表达和功能可能受LPS或细胞因子和趋化因子影响。因此,除了上述提到的NF-κB易位测定外,测量离子信号还可以洞察促炎症刺激和消炎刺激的功效。通过量化细胞内钙,钠和钾离子的浓度变化,人们可以研究刺激炎症的物质以及如何中断这一过程。
细胞内钙浓度可以使用荧光Ca2+指示剂间接成像。通常,离子敏感性荧光染料可逆地与特定离子结合,并在结合后改变其荧光特性。其中之一是FURA-2,它属于“双重激发离子指示剂”。
根据其结合状态,它改变其最大激发。Ca2+的未结合形式在380 nm处激发,而Ca2+的结合形式在340 nm处激发。通过测量510 nm处的荧光强度比,可以得出Ca2+响应。使用比率度量规避了与FURA-2浓度或细胞厚度的局部差异有关的不精确性。
为了在我们的实验室中建立比率成像的方法,为HeLa细胞建立了协议以及包括定制微分配器的特殊硬件设置。使用易于获得的ATP刺激而不是炎症的例子,可以首次测量细胞的电反应。在这里,ATP被用来引发细胞表面普遍表达的P2Y受体完成的典型生理反应。该嘌呤能受体触发钙从内质网(ER)流出进入胞质溶胶,然后可以被FURA-2检测到。图6显示了上述比例实验。
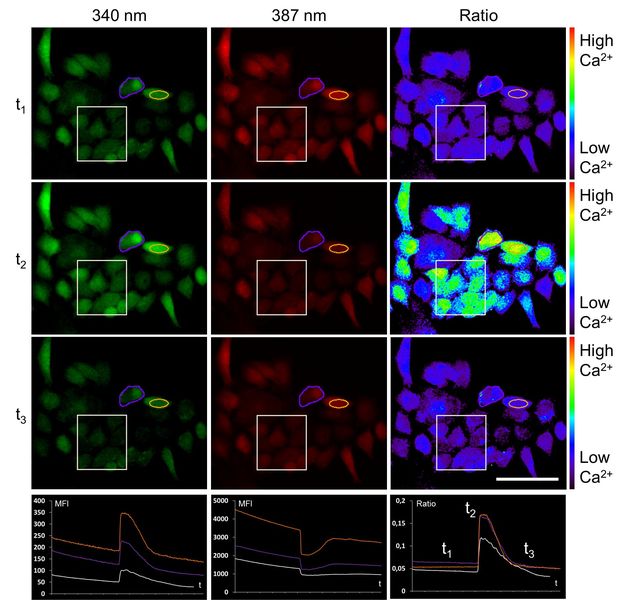
图6:为FURA成像开发了可靠的协议和硬件设置。为此,HeLa细胞装有FURA-2,并用指定波长的光激发。未刺激细胞的荧光比测量显示非常低的胞质钙浓度(时间点1,t1)。ATP刺激激活嘌呤能受体P2Y,并导致钙从ER流出到细胞质中。因此,载钙的FURA-2(例如340 nm)的荧光强度增加,不含钙的FURA-2(例如387 nm)的荧光强度降低,并且它们的比率增加(时间点2,t2)。在反应结束时,钙被运回ER,荧光比率再次降低(时间点3,t3)。成像软件LASX允许测量具有不同形状的区域的荧光强度,例如矩形(白色),椭圆形(橙色)或手绘多边形(紫色)。下排显示了不同形状内平均荧光强度(MFI)随时间以相应的颜色代码表示的变化(x轴步进10秒)。右下方的框反映了它们在指定时间点的比率。比例尺= 75μm。
加入ATP后,钙负载FURA-2(例如340 nm)的荧光强度增加,而无钙FURA-2(例如387 nm)的荧光强度降低。刺激后约100秒,钙被运回ER,FURA-2荧光活性处于原始状态。
通过比例成像的选择,可以研究钙在炎症过程中的作用,并将其分别用作炎症的指标。例如,可以用这种模型检查局部麻醉剂的抗炎能力。
在荧光显微镜下观察活细胞需要特殊的成分以保持它们的存活并处于接近自然的条件下。例如,利用温育室,可以控制适当的环境温度。为了能够调查连续盖玻片上生长的几个样品,使用了定制的样品架(见图2)。借助这种构造,可以使活细胞成像。对于活细胞成像或FURA成像的这种用途,盖玻片可以很容易地更换。
小鼠溃疡性结肠炎的研究。该疾病溃疡性结肠炎涉及结肠的慢性炎症。患者经常腹泻并有血液。长期失血可导致贫血,这些人患大肠癌的风险更高。
由于溃疡性结肠炎是一种慢性炎性疾病,因此可以假定它与TLR自由基循环有关。为了更仔细地观察,在实验室中使用了鼠标模型进行检查。有趣的是,肠道疾病可以通过将DSS混入动物的饮用水中引起。用这种饮食治疗的小鼠表现出溃疡性结肠炎的典型症状。由肠道制成的组织切片可以在明场照明下用显微镜成像。苏木精和曙红(H&E)染色使核蓝色和细胞质呈红色,可用于形态学检查小鼠结肠(图7)。
与对照组相比,经DSS处理的小鼠粘膜有严重损伤,整体上皮结构也发生了变化。而且,这些小鼠失去了粘膜的特征性内陷,即所谓的隐窝;并且通常它们的粘膜和粘膜下层被炎性细胞浸润。在上述基于细胞培养的系统之上,该小鼠模型揭示了有关生物水平上慢性炎症的结果。
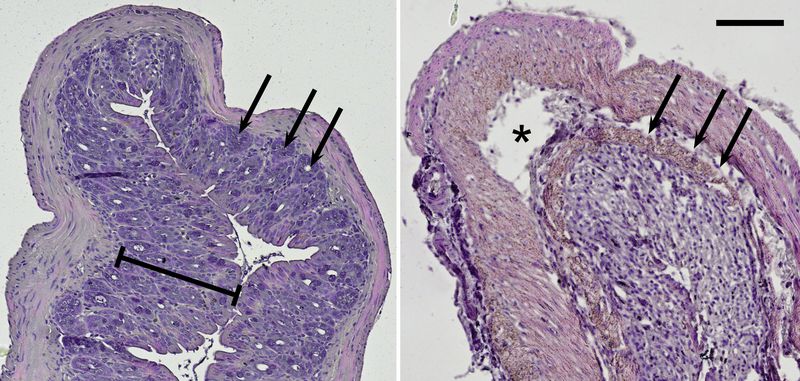
图7:通过用饮用水给予DSS,可在小鼠中诱发溃疡性结肠炎。HE染色的胆量可以在显微镜下进行组织学分析。健康的样本(左图)显示完整的粘膜(条形)和隐窝(箭头)。受影响的结肠(右图)显示出严重的破坏迹象,例如,粘膜病变(星号),整个上皮结构受损以及隐窝丢失(箭头)。对每个样本的几个单块进行成像,并借助显微镜成像软件LAS X 重新组装。比例尺= 100μm。
包括神经炎性疾病如帕金森氏病或中风在内的许多疾病,以及全身性疾病例如(自身)免疫疾病或癌症都与慢性炎症有关。了解慢性炎症的分子过程将为应对相关疾病和制定治疗策略打开新的大门。
除分子生物学外,宽视野显微镜也是一种了解TLR自由基循环(慢性炎症基础)的主要工具。例如,在常规分辨率下应用相对简单的免疫荧光显微镜观察发现,LPS刺激后,NF-κB从细胞质到细胞核的移位。NF-κB作为转录因子起作用,可增强驱动TLR自由基循环的促炎细胞因子的表达。
有趣的是,不仅LPS能够通过TLR4信号激活来启动炎症过程。还有其他来源可以间接触发TLR4信令。这些可以是例如引起自由基或直接引起DAMP产生的纳米颗粒,过渡金属,半挥发性有机化合物或臭氧。如前所述,DAMPs可以激活TLR4途径。自然,有必要进一步研究该过程并破译其背后的机制。
除了探索这个恶性循环的基本过程之外,似乎有办法破坏这种恶性循环。拥有一种用于观察NF-κB易位性(作为炎症指示)的细胞培养模型,可以检查如何阻止这种进展。我们小组目前正在研究许多草药提取物的物质,它们可能干扰转录因子向核内的转移。
除了常规分辨率的宽场荧光技术外,使用超分辨率显微镜方法甚至可以在单分子分辨率下提供有关炎症机制的更多细节。
除了蛋白质状态外,细胞的离子成分还可以提供有关炎症过程的信息。通常,离子通道对炎症反应,因为它们的表达和功能会受到细胞因子的影响。此外,例如,Ca2+通过炎症小体参与白介素的成熟。因此,它可以用作炎症进展的指标。当进行Ca2+测量时,比率FURA成像是强大的工具。建立可靠的工作系统是进一步努力破译TLR激进循环及其破坏方式的基础。将来人们可以想象筛选出会改变Ca2+反应的物质,从而对慢性炎症产生影响。
在这一点上,应该提到比例成像需要快速改变激发波长或检测到的波长,强光源,光学组件的出色透射以及快速的信号检测。超快滤光轮,经过紫外线优化的物镜,高度敏感的荧光团以及快速灵敏的摄像头(sCMOS)的开发,可以实现高空间分辨率的定量高速活细胞成像。
除了体外研究,还可以在整个生物体内研究炎症过程。因此,患有结肠慢性炎症(溃疡性结肠炎)的小鼠是有趣的研究对象。在这种情况下,其组织学状态可以用作相应组织炎症等级的指标。在此阶段,可以研究整个生物体中的慢性炎症,以及特殊饮食如何对溃疡性结肠炎产生负面或正面影响。将来,由于其氧化状态而改变其荧光行为的染料的使用将被用作ROS指示剂,以获取更多的见解。
许多不同的光学显微镜技术可用于检查潜在炎症反馈回路许多位置的慢性炎症。对比方法的范围从明场到荧光显微镜,并可以选择比例成像。检查的样品可以具有单个细胞或整个器官的大小。可以观察到固定细胞和组织学切片以及活细胞。有趣的是,对于本报告中描述的方法,研究人员对于所有不同的技术都不需要一个以上的显微镜。由于现代生命科学研究显微镜(如Leica DMi8)的灵活性和可升级性,加上用户友好的成像软件,可以从多个方向突出显示细胞过程。有了这些好处,光学显微镜在生命科学中将保持其地位,并将继续破译细胞生物学现象,并有助于对抗慢性炎症等疾病。